PMS2
From Wikipedia, the free encyclopedia
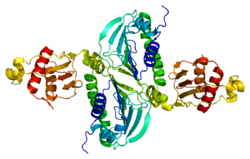
PMS2(postmeiotic segregation increased 2)は、ヒトではPMS2遺伝子にコードされる酵素(エンドヌクレアーゼ)である[4]。
ミスマッチ修復とエンドヌクレアーゼ活性
PMS2遺伝子は7番染色体上にクラスターとして存在するPMS2遺伝子ファミリーの一員である。ヒトPMS2関連遺伝子はバンド7p12、7p13、7q11、7q22に位置している。これらのホモログのエクソン1から5はPMS2と高度の同一性を示す[5]。PMS2遺伝子の産物はDNAミスマッチ修復(MMR)に関与している。PMS2タンパク質はMLH1とヘテロ二量体を形成し、この複合体はMSH2関連複合体によるミスマッチ塩基や挿入/欠失ループの認識後に活性化される。PMS2遺伝子の変異は遺伝性非ポリポーシス大腸癌(HNPCC)やターコット症候群と関係している[6]。
PMS2はミスマッチ修復に関与しており、MutLホモログに存在するmeta-binding motifの完全性に依存した潜在型エンドヌクレアーゼ活性を有することが知られている。PMS2はエンドヌクレアーゼとして、非連続的なDNA鎖にさらにニックを導入する[7]。
相互作用
PMS2はMLH1と相互者王してMutLαヘテロ二量体を形成することが示されている[8][9][10][11][12][13]。MLH1上の相互作用ドメイン(492–742番残基)をめぐって、MLH3、PMS1、PMS2の間には競合が存在する[9]。
PMS2の相互作用ドメインにはロイシンジッパータンパク質に特徴的なヘプタッドリピートが存在し、MLH1の506–756番残基と相互作用する[10]。
MutSヘテロ二量体(MutSαやMutSβ)は、ミスマッチ部位への結合に伴ってMutLαと結合する。MutLαは、ミスマッチ認識段階からその他の過程、すなわち新生DNA鎖からのミスマッチの除去、分解されたDNAの再合成、DNA中のニックの修復などへの連結を担っていると考えられている[13]。MutLαは弱いATPアーゼ活性を持つことが示されており、また非連続的なDNA鎖にさらにニックを導入するエンドヌクレアーゼ活性も持つ。これによって、EXO1によるミスマッチDNA鎖の5'→3'方向の分解が促進される[13]。MutLαの活性部位はPMS2サブユニットに位置する。PMS1とPMS2はMLH1との相互作用をめぐって競合する[13]。タンデムアフィニティ精製によって、PMS2と相互作用するタンパク質群が同定されている[13][14]。ヒトのPMS2は極めて低レベルで発現しており、細胞周期の強力な制御下には置かれていないと考えられている[15]。
p53やp73との相互作用
PMS2はp53やp73と相互作用することが示されている。p53が存在しない場合でも、PMS2が欠損した細胞と機能している細胞の双方でシスプラチン処理時の細胞周期のG2/M期チェックポイントでの停止は機能しているが、p53とPMS2の双方を欠損した細胞では抗がん剤に対する感受性が増大する[16]。PMS2はp53欠損細胞において細胞生存の媒介因子となっており、p53非依存的にDNA損傷応答を調節する[16]。PMS2とMLH1はミスマッチ修復に依存した形で、p73を介したアポトーシスに対抗することで細胞死からの保護を行う[16]。一方で、PMS2はp73と相互作用し、p73を安定化することでシスプラチン誘発性アポトーシスを促進する。シスプラチンはPMS2とp73の相互作用を促進し、この作用はc-Ablに依存している[12]。MutLα複合体はp73を損傷DNA部位へリクルートするアダプターとして機能している可能性があり、その中でPMS2はp73の活性化因子として作用している可能性がある。PMS2の過剰発現は、MLH1非存在下、p73とシスプラチンの存在下において、PMS2のp73に対する安定化作用によりアポトーシスを促進している可能性がある[12]。DNA損傷時には、p53はp21/WAF経路を介して細胞周期の停止を誘導し、MLH1とPMS2の発現によって損傷修復を開始する[11]。MutLα複合体はDNA損傷の程度のセンサーとして機能し、損傷が修復能力を超えた場合にはp73を安定化してアポトーシスを開始すると考えられている[11]。また、MLH1はMLH3やPMS1とも複合体を形成することができるため、PMS2の喪失は必ずしもMLH1の不安定性をもたらすわけではない[17]。