トレミフェン
From Wikipedia, the free encyclopedia
発音
[ˈtɔːrəmɪfiːn]
商品名
Fareston, others
その他名称
(Z)-Toremifene; 4-Chlorotamoxifen; 4-CT; Acapodene; CCRIS-8745; FC-1157; FC-1157a; GTx-006; NK-622; NSC-613680
 | |
 | |
| 臨床データ | |
|---|---|
| 発音 | [ˈtɔːrəmɪfiːn] |
| 商品名 | Fareston, others |
| その他名称 | (Z)-Toremifene; 4-Chlorotamoxifen; 4-CT; Acapodene; CCRIS-8745; FC-1157; FC-1157a; GTx-006; NK-622; NSC-613680 |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a608003 |
| 医療品規制 | |
| 投与経路 | 経口投与 |
| 薬物クラス | 選択的エストロゲン受容体修飾薬 |
| ATCコード | |
| 薬物動態学データ | |
| 生体利用率 | Good/~100%[1][2] |
| タンパク結合 | 99.7%[1] |
| 代謝 | 肝臓 (CYP3A4)[3][2] |
| 代謝物質 | N-デスメチルトレミフェン; 4-ヒドロキシトレミフェン; オスペミフェン[4][5] |
| 消失半減期 |
トレミフェン: 3–7 日[1] 代謝物: 4–21 日[2][5][1] |
| 排泄 | 糞便: 70% (代謝物として)[2] |
| 識別子 | |
| |
| CAS登録番号 |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB ligand | |
| CompTox ダッシュボード (EPA) | |
| ECHA InfoCard | 100.125.139 |
| 化学的および物理的データ | |
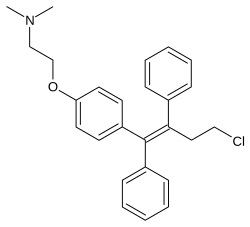
| 化学式 | C26H28ClNO |
| 分子量 | 405.97 g·mol−1 |
| 3D model (JSmol) | |
| |
|
| |
| (verify) | |
トレミフェンクエン酸塩(Toremifene citrate)は経口選択的エストロゲン受容体調節薬(SERM)の一つであり、体内で抗エストロゲン作用を発揮する。日本では「閉経後乳癌」治療薬として1995年3月に承認された[6]。米国では進行(転移性)乳癌治療薬として1997年5月に承認された[7]:Approval History。前立腺癌治療薬としての効果も検討されている[8]。商品名フェアストン。
トレミフェンは下記の患者に禁忌である[9]。
- 妊婦または妊娠している可能性のある婦人および授乳婦
- QT延長またはその既往歴のある患者(先天性QT延長症候群等)
- 低カリウム血症の患者
- クラスIA(キニジン、プロカインアミド等)またはクラスIII(アミオダロン、ソタロール等)の抗不整脈薬を投与中の患者