ヒドラゾン
From Wikipedia, the free encyclopedia
合成
通常は、ケトンとヒドラジンの脱水縮合で合成する。
- R1C(=O)R2 + H2N-NR3R4 → R1C(=N-NR3R4)R2
カルバニオンとジアゾニウムイオンが結合してできるアゼン (azene) が互変異性化するとヒドラゾンとなる。
- EE'CH− + +N2Ar → EE'CH-N=N-Ar (アゼン) → EE'C=N-NHAr (E,E' = 電子求引基)
上の例は活性メチレン化合物の反応であるが、活性メチン化合物を基質とした場合は電子求引基が脱離した生成物が得られる場合があり、ヤップ・クリンゲマン反応 (Japp-Klingemann reaction) と呼ばれる。
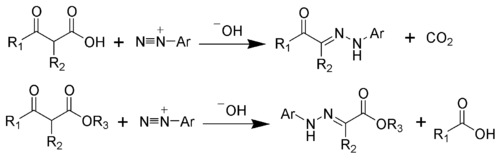
反応
イミンやカルボニル化合物と同様に、炭素上が電子不足になっているために求核剤の攻撃を受ける。求核剤が水や水酸化物イオンである場合が加水分解である。
求電子剤は反対側の窒素を攻撃する。例えば、ハロゲン化アルキルでアルキル化することができる。
- R(R')C=N-NH2 + R''-CHO → R(R')C=N-N=CHR'' (アジン)
ヒドラゾンに水素化リチウムアルミニウムを作用させると水素化を受けてヒドラジンとなる。
- R(R')C=N-NH2 + LiAlH4 → R(R')CH-NH-NH2
酸化銀(I) で脱水素させ、ジアゾ化物に変える反応がある。
- (H3C)2C=N-NH2 + Ag2O → (H3C)2C=N2
ウォルフ・キッシュナー還元では、ケトンとヒドラジンから最初にヒドラゾンができ、さらなる強塩基の作用により窒素分子が脱離してメチレン化合物に変わる。
ヒドラゾンはまた、フィッシャーのインドール合成やエッシェンモーザー・タナベ開裂の中間体として知られる。
