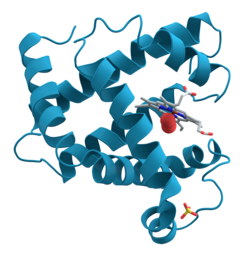
ミオグロビン
From Wikipedia, the free encyclopedia
構造と機能
1本のポリペプチド鎖と1分子のヘムからなり、酸素分子を結合する。筋繊維中に広く見られ、球状タンパクで酸素を蓄える。153個のアミノ酸残基から成り、1個のヘムをもち、分子量は約1万7800である。タンパク質は8個のαヘリックスをもち、それらがヘムをとり囲んでいる。酸素分子はヘムの中央にある鉄に可逆的に結合する(酸素化)。
- 酸素の貯蔵(Long period oxygen storage)[1][2]
- 生体触媒(Biochemical catalyst)[3][2]
- 酸素透過の促進(Facilitation of oxygen diffusion)[4][2]
- 酸素バッファー(Oxygen bufferあるいはShort-time oxygen storage)[2]
酸素に対する化学親和力がヘモグロビンより高く、血中のヘモグロビンから酸素を受け取り貯蔵することができる。ミオグロビンの構造と機能はヘモグロビンと類似性が高いが、ヘモグロビンが四量体であるのに対してミオグロビンは単量体である点が大きく異なっている。外部酸素濃度が低い場合、例えば筋肉の酸素要求が血液からの供給を超えた場合などにのみ酸素分子を放出し、緊急時の酸素貯蔵庫として機能する。