Octabisvalen
chemische Verbindung
From Wikipedia, the free encyclopedia
Octabisvalen ist eine chemische Verbindung aus der Gruppe der gesättigten polycyclischen Kohlenwasserstoffe. Neben Cuban und Cunean ist Octabisvalen ein Vertreter der drei möglichen gesättigten C8H8-Kohlenwasserstoffe und ein Valenzisomer von Cyclooctatetraen.[3][4]
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
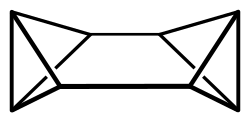 | ||||||||||
| Allgemeines | ||||||||||
| Name | Octabisvalen | |||||||||
| Andere Namen |
Pentacyclo[5.1.0.02,4.03,5.06,8]octan (IUPAC) | |||||||||
| Summenformel | C8H8 | |||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 104,15 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Schmelzpunkt |
27–30 °C[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Darstellung
Die Darstellung der ersten Verbindung mit einer Octabisvalenstruktur wurde 1985 von Christoph Rücker und Horst Prinzbach publiziert.[4] In einer ursprünglich elfstufigen Synthesesequenz, die auf acht Stufen verkürzt werden konnte, sind präparativ brauchbare Mengen (Z)-3,7-Bis(phenylsulfonyl)octabisvalen zugänglich:[5]
Durch Umsetzung von syn-Benzoltrioxid 2 mit Methylphenylsulfon[S 1] 1 und n-Butyllithium erhält man in fast quantitativer Ausbeute ein intramolekular cyclisiertes Bisadditionsprodukt 3, das im Folgeschritt mit Aceton in Gegenwart von p-Toluolsulfonsäure zum Acetal 4 umgesetzt wird. Die verbliebene Hydroxygruppe wird mit Methansulfonsäurechlorid in das Mesylat 5 überführt, das mit n-Butyllithium und Diisopropylamin in THF zum Zwischenprodukt 6 cyclisiert. Nach dem Abspalten der Schutzgruppe mit Salzsäure in Methanol zum Diol 7 werden die beiden Hydroxygruppen mit Benzolsulfonsäurechlorid in Gegenwart von Triethanolamin in den Benzolsulfonsäureester überführt. Zwischenprodukt 8 wird mit n-Butyllithium in THF zur tetracyclischen Verbindung 9 umgesetzt, die mit Kaliumhydroxid in DMSO zum (Z)-3,7-Bis(phenylsulfonyl)octabisvalen 10 cyclisiert.[6]
Die Darstellung des unsubstituierten Octabisvalen durch Umsetzung von (Z)-3,7-Bis(phenylsulfonyl)octabisvalen mit Natrium in flüssigem Ammoniak wurde 1987 beschrieben.[1] Als weitere Variante gelingt die Darstellung der Verbindung durch eine analoge Umsetzung eines cyanosubstiturierten Octabisvalen, das sich wiederum in einer fünfstufigen Reaktion aus Tricyclo[4.1.0.00,7]hept-4-en-3-on[S 2] herstellen lässt.[7]
Eigenschaften
Das Octabisvalenmolekül besitzt eine D2h-Symmetrie und weist mit den beiden Bicyclo[1.1.0]butan-Einheiten eine hohe Ringspannung auf. Die MM2-Kraftfeldrechnung von Octabisvalen ergibt eine Ringspannungsenergie von 644 kJ/mol, ein Wert der zwischen der Ringspannung von Cuban (694 kJ/mol) und Cunean (571 kJ/mol) liegt. Bis zu einer Temperatur von 140 °C ist Octabisvalen thermisch inert.[1]
Nach der IUPAC-Nomenklatur kann bei Octabisvalen nicht zwischen der 7- und der 8-Position unterschieden werden. Daraus folgt, dass es für 3,7-disubstituierte Octabisvalenderivate zwei Stereoisomere gibt, für die in Anlehnung an die (Z)/(E)-Isomerie bei den Alkenen ebenfalls die Bezeichnung (Z)- und (E)-Isomer vorgeschlagen wurde.[8]
1991 wurde die Synthese von heterocyclischen Octabisvalenen, dem (Z)-7-Cyano-3-azaoctabisvalen und dem (Z)-3,7-Diazaoctabisvalen, veröffentlicht.[9]




