Ferroceno
From Wikipedia, the free encyclopedia
| Ferroceno | ||
|---|---|---|
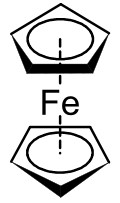 | ||
 | ||
| Nombre IUPAC | ||
| bis(η5-ciclopentadienil)hierro | ||
| General | ||
| Fórmula semidesarrollada | [Fe(η5-C5H5)2] | |
| Fórmula molecular | C10H10Fe | |
| Identificadores | ||
| Número CAS | 102-54-5[1] | |
| Número RTECS | LK0700000 | |
| ChemSpider | 7329 | |
| PubChem | 504306 7611, 504306 | |
| UNII | U96PKG90JQ | |
| Propiedades físicas | ||
| Apariencia | Polvo cristalino naranja | |
| Densidad | 2690 kg/m³; 2,69 g/cm³ | |
| Masa molar | 186,04 g/mol | |
| Punto de fusión | 447 K (174 °C) | |
| Punto de ebullición | 522 K (249 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | insoluble | |
| Peligrosidad | ||
| SGA |
   | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ferroceno es un compuesto organometálico cuya fórmula es [Fe(η5-C5H5)2]. Es el prototipo de los metalocenos, un grupo de compuestos organometálicos cuya estructura se basa en una disposición centrada del metal entre dos aniones ciclopentadienilos enfrentados entre sí, los cuales dan gran estabilidad al compuesto. Estos compuestos son también conocidos como compuestos sandwich.[2] El rápido crecimiento de la Química organometálica se atribuye a menudo al entusiasmo que proviene del descubrimiento de ferroceno y sus muchos análogos.
El ferroceno se preparó por primera vez sin quererlo. En 1951, Pauson y Kealy en la Universidad Duquesne informaron de la reacción del bromuro de ciclopentadienilmagnesio y el cloruro de hierro (III) con el objetivo de acoplar oxidativamente el dieno para preparar fulvaleno:


En cambio, obtuvo un polvo de color naranja claro de “notable estabilidad”.[3]
Publicaron la descripción de la síntesis de un compuesto inusual de hierro con dos anillos ciclopentadieno unidos iónicamente al átomo de hierro. Esta estabilidad estaba de acuerdo con el carácter aromático de los ciclopentadienilos cargados negativamente, pero la estructura sándwich del compuesto η5 (pentahapto) no fue reconocida por ellos. También Miller, Tebboth y Tremaine sintetizaron el ferroceno por una vía diferente, a partir de una reacción del ciclopentadieno con hierro en presencia de aluminio, potasio, o de óxidos de molibdeno[4]
Años más tarde, Robert Burns Woodward y Geoffrey Wilkinson descubrieron que la estructura propuesta era incorrecta y dedujeron la estructura sobre la base de:[5]
Woodward predijo la aromaticidad del ferroceno y su confirmación por reacciones de sustitución electrófila aromática. Esta similitud con el benceno fue lo que le hizo llamar al compuesto como ferroceno.
Independientemente Ernst Otto Fischer también llegó a la conclusión de la estructura de sandwich y empezó a sintetizar otros metalocenos como el niqueloceno y el cobaltoceno.[6] La estructura del ferroceno fue confirmada por:
- NMR.
- Espectroscopia y cristalografía de rayos X.[7][8]
Su distintiva estructura "sándwich" llevó a una explosión de interés en los compuestos de metales bloque d con los hidrocarburos, y revitalizar el desarrollo del floreciente estudio de la química organometálica. En 1973, Fischer de Technische Universität München y Wilkinson del Imperial College de Londres compartieron un Premio Nobel por su trabajo sobre los metalocenos y otros aspectos de la química organometálica.[9]
Estructura y enlace
Al átomo de hierro en el ferroceno se le asigna normalmente el estado de oxidación +2, como se puede demostrar usando la espectroscopia Mössbauer. A cada ciclopentadienilo (Cp) del anillo se le asigna una carga negativa, con 6 electrones-π en cada anillo, y convirtiéndolos así en aromáticos al cumplir con la regla de Hückel. Estos doce electrones se comparten con el metal a través de enlaces covalentes, que, junto con los seis electrones d del Fe2+, resulta un complejo que tiene 18 electrones, cumpliendo así con la regla de los 18 electrones.
La falta de uniones individuales entre los átomos de carbono del anillo (Cp) y el ion Fe2+ hace que los anillos de Cp puedan rotar libremente sobre el eje Cp(centroide)-Fe-Cp(centroide), como se ha observado por resonancia magnética nuclear.[10] y microscopía de efecto túnel.[11][12]
Las distancias de enlace carbono-carbono son de 1,40 Å dentro de los anillos de Cp, y las distancias de enlace entre el hierro intercalado y los carbonos de los anillos son de 2,04 Å.

La conformación eclipsada se encuentra en la naturaleza junto con la conformación alternada.[13] El ferroceno cristaliza en un sistema cristalino monoclínico a temperatura ambiente, a T <164 K en el triclínico y a T <110 K en el ortorrómbico. En la forma monoclínica se tiene una conformación alternada (con una geometría D5d) son moléculas de ferroceno cuyos anillos de ciclopentadienilo no están alineados en el eje de simetría principal (el que une los centros de los anillos a través del metal). El sistema triclínico difiere en 9° de la disposición eclipsada (tiene una geometría D5), y la forma ortorrómbica (D5h) está construida totalmente eclipsada.[14][15]
El ferroceno en fase gas se encuentra en la forma eclipsada, aunque la barrera energética de rotación es muy pequeña. El ferroceno metil-sustituido en todas las posiciones de los anillos (el decametilferroceno o [Cp(CH3)5]2Fe), sin embargo, se encuentra en la conformación alternada tanto cristalizado como en fase gas.
Propiedades físicas

El ferroceno es un sólido naranja estable al aire que sublima fácilmente, especialmente después de calentamiento en el vacío. Como era de esperar para una especie simétrica y sin carga, el ferroceno es soluble en disolventes orgánicos apolares, como el benceno, pero es insoluble en agua. Es estable a temperaturas tan altas como 400 °C.[16]
La siguiente tabla muestra los valores típicos de la presión de vapor del ferroceno a diferentes temperaturas:[17]
Presión (Pa) 1 10 100 Temperatura (K) 298 323 353
Preparación
Para formar metalocenos, se utiliza ciclopentadienuro sódico y el haluro metálico que interese. En este caso, el ferroceno se prepara eficientemente por reacción de ciclopentadienuro de sodio y cloruro de hierro (II) anhidro en disolventes etéreos.[18] El ferroceno se obtiene finalmente por sublimación.
- 2 NaC5H5 + FeCl2 → Fe(C5H5)2 + 2 NaCl
En el laboratorio se puede preparar el ciclopentadienuro, de forma alternativa, usando hidróxido de potasio sobre ciclopentadieno, obteniendo así el ciclopentadienuro de potasio.
Reacciones
Con electrófilos

El ferroceno sufre muchas reacciones características de los compuestos aromáticos, lo que permite la preparación de sus derivados sustituidos. Así pues, será importante la sustitución electrófila aromática. Un experimento común es la reacción de Friedel-Crafts de ferroceno con anhídrido acético (o cloruro de acetilo) en presencia de ácido fosfórico como catalizador. La preparación de derivados de fósforo de ferrocenos son ilustrativos. En presencia de cloruro de aluminio, el Me2NPCl2 y el ferroceno reaccionan para dar ferrocenil dicloro fosfina,[19] mientras que el tratamiento con fenilciclorofosfina en condiciones similares forma p, p-diferrocenil-p-fenil fosfina.[20] En común con el anisol la reacción del ferroceno con P4S10 forma un ditiodifosfetano disulfuro.[21]
Litiación
El ferroceno reacciona fácilmente con el butil-litio para dar 1,1 '-dilitioferroceno, que a su vez es un versátil nucleófilo. Se ha informado que la reacción del 1,1'-dilitioferroceno con dietil ditiocarbamato de selenio forma un tenso ferrocenofano donde los dos ligandos ciclopentadienilo están unidos por el átomo de selenio.[22]
Este ferrocenofano se puede convertir en un polímero por una polimerización por apertura del anillo térmica para formar (ferrocenilseleniuro). Asimismo por la reacción de silicio y fósforo unido a ferrocenofanos se puede obtener los poli(ferrocenilsilano)s y los poli(ferrocenilfosfina)s.[23][24]
Química redox

A diferencia de la mayoría de los hidrocarburos, el ferroceno se somete a una oxidación electrónica a bajo potencial, alrededor de 0,5 V vs. un electrodo de calomelanos saturado (SCE). Algunos hidrocarburos ricos en electrones (por ejemplo, la anilina) también se oxidan a bajos potenciales, pero solo irreversiblemente. La oxidación del ferroceno da un catión estable llamado ferrocenio. En una escala preparativa, la oxidación se efectúa convenientemente con FeCl3 para dar el ion de color azul, [Fe(C5H5)2]+, que es a menudo aislado, como su sal PF6-. Alternativamente, el nitrato de plata puede ser utilizado como oxidante.
Las sales de Ferrocenio a veces se utilizan como agentes oxidantes, en parte porque el producto ferroceno es bastante inerte y fácilmente separable de los productos iónicos.[25] Los sustituyentes en los ligandos ciclopentadienilo alteran el potencial redox de la forma esperada: grupos que retiran electrones tales como un ácido carboxílico cambian el potencial en la dirección anódica (es decir,, cada vez más positiva), mientras que los grupos que liberan electrones tales como los grupos metil cambian el potencial en la dirección catódica (más negativo). Así, el decametilferroceno es mucho más fácil de oxidar que el propio ferroceno. El ferroceno se utiliza a menudo como un patrón interno para calibrar los potenciales redox en electroquímica no acuosa.
Estereoquímica
Una variedad de patrones de sustitución son posibles con el ferroceno incluyendo la sustitución en uno o ambos de los anillos. Los patrones de sustitución más comunes son los 1-sustituidos (un sustituyente en un anillo) y 1,1'-disustituidos (un sustituyente en cada anillo). Por lo general los anillos pueden girar libremente, lo que simplifica la isomería.
Los ferrocenos disustituidos pueden existir en cualquiera de los isómeros 1,2- y 1,1', que no son interconvertibles. Los 1,2-ferrocenos heterodisustituidos son quirales.


