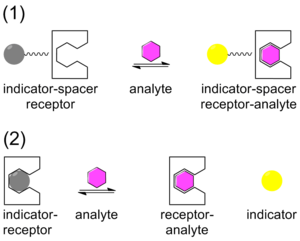
Chimie hôte-invité
From Wikipedia, the free encyclopedia
En chimie supramoléculaire[1], la chimie hôte-invité décrit des complexes qui sont composés de deux ou plusieurs molécules ou ions qui sont maintenus ensemble par des forces autres que celles des liaisons covalentes. La chimie hôte-invité englobe l'idée de la reconnaissance moléculaire et des interactions par liaison non-covalente. Cette dernière est essentielle pour maintenir la structure 3D de grandes molécules, telles que les protéines, et est impliquée dans de nombreux processus biologiques dans lesquels de grandes molécules se lient spécifiquement mais de manière transitoire les unes aux autres.
Bien que les interactions non-covalentes puissent être grossièrement divisées en celles ayant des contributions plus électrostatiques ou dispersives, il existe d'autres types d'interactions non-covalentes : liaison ionique, liaison hydrogène, forces de van der Waals et interactions hydrophobes[2].

La chimie hôte-invité est une branche de la chimie supramoléculaire dans laquelle une molécule hôte forme un composé chimique avec une molécule ou un ion invité. Les deux composants du complexe sont maintenus ensemble par des forces non-covalentes, le plus souvent par liaison hydrogène. La liaison entre l'hôte et l'invité est généralement très spécifique aux deux parties concernées. La formation de ces complexes est au cœur du sujet de la reconnaissance moléculaire.
Il existe un équilibre entre l'état non lié, dans lequel l'hôte et l'invité sont séparés l'un de l'autre, et l'état lié, dans lequel ils forment un complexe hôte-invité défini structurellement :
- H = « hôte », G = « invité », HG = « complexe hôte-invité »
Le composant « hôte » peut être considéré comme la plus grande molécule, et il englobe la plus petite molécule « invitée ». Dans les systèmes biologiques, les termes analogues d'hôte et d'invité sont communément appelés « enzyme » et « substrat »[5].
Afin de concevoir des systèmes synthétiques qui exécutent des fonctions et des tâches spécifiques, il est très important de comprendre la thermodynamique de la liaison entre l'hôte et l'invité. Les chimistes se concentrent sur l'échange d'énergie de différentes interactions de liaison et tentent de développer des expériences scientifiques pour quantifier les origines fondamentales de ces interactions non-covalentes en utilisant diverses techniques telles que la spectroscopie RMN, la spectroscopie ultraviolet-visible et la calorimétrie de titrage isotherme[6]. L'analyse quantitative des valeurs constantes de liaison fournit des informations thermodynamiques utiles[5].
Principes thermodynamiques des interactions hôte-invité
Les avantages thermodynamiques de la chimie hôte-invité viennent de l'idée qu'il existe une énergie libre de Gibbs globale plus faible en raison de l'interaction entre les molécules hôtes et invitées. Les chimistes tentent de mesurer l'énergie et les propriétés thermodynamiques de ces interactions non-covalentes; et ce faisant, nous espérons avoir un meilleur aperçu du résultat combinatoire de ces nombreuses petites forces non-covalentes qui sont utilisées pour générer un effet global sur la structure supramoléculaire.
Une constante d'association peut être définie par l'expression
où {HG} est l'activité thermodynamique du complexe à l'équilibre. {H} représente l'activité de l'hôte et {G} représente l'activité de l'invité. Les quantités , et sont les concentrations et est un quotient des coefficients d'activité.
En pratique, la constante d'équilibre est généralement définie en termes de concentrations :
Lorsque cette définition est utilisée, il est sous-entendu que le quotient des coefficients d'activité a une valeur numérique de 1. Il apparaît alors que la constante d'équilibre a la dimension 1/concentration, mais cela ne peut pas être vrai puisque le changement d'énergie libre standard de Gibbs, est proportionnel au logarithme de K.
Ce paradoxe est résolu lorsque la dimension de est définie comme l'inverse de la dimension du quotient des concentrations. Le facteur est considéré comme ayant une valeur constante dans toutes les conditions expérimentales pertinentes. Néanmoins, il est courant d'attacher une dimension, telle que millimole par litre ou micromole par litre, à une valeur de K qui a été déterminée expérimentalement.
Une grande valeur de indique que les molécules hôtes et invitées interagissent fortement pour former le complexe hôte-invité.
Détermination des valeurs de constantes de liaison
Complexation simple hôte-invité
Lorsque les molécules hôtes et invitées se combinent pour former un seul complexe, l'équilibre est représenté par
et la constante d'équilibre, K, est définie comme
où [X] désigne la concentration d'une espèce chimique X (tous les coefficients d'activité sont supposés avoir une valeur numérique de 1). Les équations, à tout point de données,
où et représentent les concentrations totales de l'hôte et de l'invité, peuvent être réduites à une seule équation quadratique et, par exemple, [G] et peuvent donc être résolues analytiquement pour toute valeur donnée de K. Les concentrations [H] et [HG] peuvent alors être dérivées.
La prochaine étape consiste à calculer la valeur, , d'une quantité correspondant à la quantité observée . Ensuite, une somme de carrés, U, sur tous les points de données, np, peut être définie comme
et cela peut être minimisé par rapport à la valeur de constante de stabilité, K, et à un paramètre tel que le déplacement chimique du complexe HG (données RMN) ou son absorbance molaire (données UV/visible). La minimisation peut être effectuée dans une application de feuille de calcul telle qu'Excel à l'aide de l'utilitaire Solver intégré.
Cette procédure ne doit être utilisée que lorsqu'il est certain que l'adduit 1:1 est la seule espèce complexe formée. Un simple contrôle de la validité de cette assertion est que les résidus devraient montrer une distribution aléatoire ; sinon, la formation d'une seconde espèce doit être envisagée.
Calorimétrie
La chaleur dégagée lorsqu'une aliquote de solution hôte est ajoutée à une solution contenant l'invité est la somme des contributions de chaque réaction telle que
où est une valeur de changement de chaleur mesurée (corrigée pour toutes les contributions de chaleur étrangères) au point de données j. est la quantité de chaleur absorbée ou émise lorsqu'une mole du ième produit de réaction est formée et est le changement réel du nombre de moles de ce produit à ce point de données. est calculé en résolvant les équations du bilan massique avec des valeurs données des constantes d'équilibre. Si les valeurs de la constante d'équilibre sont connues, le changement d'enthalpie standard peut être calculé par un processus linéaire des moindres carrés, sinon une méthode non linéaire d'ajustement des données doit être utilisée.
La calorimétrie par titrage isotherme est couramment utilisée pour déterminer les valeurs à la fois d'une constante d'équilibre et de l'enthalpie de réaction standard correspondante. Les fabricants d'instruments fournissent certains logiciels avec lesquels ces quantités peuvent être obtenues à partir de valeurs de données expérimentales.
Réaction de complexation générale
Pour chaque équilibre impliquant un hôte, H, et un invité G :
la constante d'équilibre, , est définie comme
Les valeurs des concentrations libres et sont obtenus en résolvant les équations avec des valeurs connues ou estimées pour les constantes de stabilité.
Ensuite, les concentrations de chaque espèce complexe peuvent également être calculées comme . La relation entre la concentration d'une espèce et la quantité mesurée est spécifique à la technique de mesure, comme indiqué dans chaque section ci-dessus. En utilisant cette relation, l'ensemble de paramètres, les valeurs de constantes de stabilité et les valeurs de propriétés telles que l'absorbance molaire ou les déplacements chimiques spécifiés, peuvent être affinés par un processus de raffinement non linéaire des moindres carrés. Pour une présentation plus détaillée de la théorie, voir Détermination des constantes d'équilibre. Certains programmes informatiques dédiés sont répertoriés dans des logiciels.
Techniques expérimentales
Résonance magnétique nucléaire
La résonance magnétique nucléaire (RMN) est l'une des techniques spectroscopiques les plus puissantes en chimie analytique. C'est un outil important pour l'étude des complexes hôte-invité, pour élucider les structures des différents complexes existant sous forme d'agrégats, de paires d'ions ou de systèmes encapsulés. Comme son nom l'indique, la RMN identifie les différents noyaux des molécules (le plus souvent, le proton), en mesurant leur déplacement chimique. L'association entre deux molécules entraîne une modification considérable de leurs environnements électroniques. Cela conduit à un déplacement des signaux dans le spectre RMN, et ce principe de base est utilisé pour étudier les phénomènes de chimie hôte-invité. Les forces motrices de la liaison hôte-invité sont les diverses interactions secondaires entre les molécules, telles que la liaison hydrogène et l'interaction pi. Ainsi, la RMN sert également de technique importante pour établir la présence de ces interactions dans un complexe hôte-invité[7].

Des études de RMN ont donné des informations utiles sur la liaison de différents invités aux hôtes. Fox et al.[8] ont calculé les interactions de liaison hydrogène entre les molécules de pyridine et de dendrimère poly(amidoamine) (PAMAM), sur la base du déplacement chimique de l'amine et des groupes amide. Dans une étude similaire, Xu et al.[9] titré le dendrimère G4 PAMAM à base de carboxylate (l'hôte) avec divers médicaments à base d'amine (les invités) et surveillé les déplacements chimiques du dendrimère. En conjonction avec les techniques de RMN 2D-NOESY, ils ont pu localiser précisément la position des médicaments sur les dendrimères et l'effet de la fonctionnalité sur l'affinité de liaison des médicaments. Ils ont trouvé des preuves concluantes pour montrer que les molécules de médicaments cationiques se fixent à la surface des dendrimères anioniques par des interactions électrostatiques, alors qu'un médicament anionique se localise à la fois dans le noyau et la surface des dendrimères, et que la force de ces interactions dépend des valeurs de pKa des molécules.
Dans une autre étude, Sun et al.[9] ont étudié la chimie hôte-invité des molécules de ruthénium trisbipyridyl-viologène avec le cucurbiturile. Tout en étudiant le changement des déplacements chimiques des protons de pyridine sur le viologène, ils ont constaté que les modes de liaison pour les complexes 1:1 sont complètement différents pour les différentes molécules de cucurbiturile.
Un facteur important à garder à l'esprit lors de l'analyse de la liaison entre l'hôte et l'invité est le temps nécessaire à l'acquisition des données par rapport au temps de l'événement de liaison. Dans de nombreux cas, les événements de liaison sont beaucoup plus rapides que l'échelle de temps d'acquisition des données, auquel cas le résultat est un signal moyenné pour les molécules individuelles et le complexe. L'échelle de temps RMN est de l'ordre de la milliseconde, ce qui dans certains cas lorsque la réaction de liaison est rapide, limite la précision de la technique[5].
Spectroscopie ultraviolet-visible

La spectroscopie ultraviolet-visible est l'une des méthodes les plus anciennes et les plus rapides pour étudier l'activité de liaison de diverses molécules. L'absorption de la lumière UV a lieu à une échelle de temps de 1 × 10−12 s (une picoseconde), d'où les signaux individuels de l'espèce peuvent être observés. Dans le même temps, l'intensité de l'absorption est directement corrélée à la concentration de l'espèce, ce qui permet un calcul facile de la constante d'association[5]. Le plus souvent, l'hôte ou l'invité est transparent aux rayons UV, tandis que l'autre molécule est sensible aux UV. L'évolution de la concentration des molécules sensibles aux UV est ainsi suivie et ajustée en ligne droite par la méthode de Benesi-Hildebrand (en), à partir de laquelle la constante d'association peut être directement calculée.
Des informations supplémentaires sur la stœchiométrie des complexes sont également obtenues, car la méthode de Benesi-Hildebrand suppose une stœchiométrie 1:1 entre l'hôte et l'invité. Les données traceront une ligne droite seulement si la formation complexe suit également une stœchiométrie 1:1 similaire. Un exemple récent d'un calcul similaire a été effectué par Sun et al.[9], dans lequel ils ont titré des molécules de ruthénium trisbipyridyl-viologène avec des urilles de cucurbitacées. Ils ont tracé l'absorbance relative des molécules de cucurbitacées en fonction de leur concentration totale à une longueur d'onde spécifique. Les données ont bien adapté un modèle de liaison 1:1 avec une constante de liaison de 1,2 × 105 M−1.
En tant qu'extension, on peut adapter les données à différentes stœchiométrie pour comprendre la cinétique de liaison entre l'hôte et l'invité[10] se sont servis de ce corollaire pour modifier légèrement le tracé Benesi-Hildebrand conventionnel pour obtenir l'ordre de la réaction de complexation entre le complexe hétérotrinucléaire salen (en) Zn(II) chiral ponté par l'éther couronne contenant du baryum (hôte) avec divers invités imidazoles et esters méthyliques d'acides aminés, ainsi que les autres paramètres. Ils ont titré une concentration fixe du complexe de zinc avec des quantités variables d'imidazoles et d'esters méthyliques tout en surveillant les changements de l'absorbance de la bande de transition pi-pi* à 368 nm. Les données correspondent à un modèle dans lequel le rapport invité-hôte est de 2 dans le complexe. Ils ont ensuite mené ces expériences à différentes températures qui leur ont permis de calculer les différents paramètres thermodynamiques à l'aide de l'équation de van 't Hoff.
Calorimétrie par titrage isotherme
Les techniques spectroscopiques donnent les valeurs de la constante de liaison et l'énergie libre de Gibbs, . Pour obtenir l'ensemble complet des paramètres thermodynamiques tels que et , une analyse de van 't Hoff utilisant l'équation de van 't Hoff serait nécessaire. Cependant, les progrès récents des techniques calorimétriques permettent de mesurer et en une seule expérience, permettant ainsi de déterminer tous les paramètres thermodynamiques à l'aide de l'équation :
à condition que l'expérience soit réalisée dans des conditions isothermes. La procédure est similaire à une procédure de titrage conventionnelle dans laquelle l'hôte est ajouté séquentiellement à l'invité et la chaleur absorbée ou dégagée est mesurée, comparée à une solution à blanc. La chaleur totale dégagée, Q, correspond à la constante d'association, , et par l'équation :
Ce qui peut être simplifié comme
où
- : concentration molaire initiale de l'hôte,
- : concentration molaire de l'invité,
- : volume du récipient.
L'équation ci-dessus peut être résolue par une analyse de régression non linéaire pour obtenir les valeurs de et et par la suite de et pour cette réaction particulière[5]. Les avantages de la calorimétrie par titrage isotherme par rapport aux autres techniques couramment utilisées, outre le fait de donner l'ensemble des paramètres thermodynamiques, sont qu'elle est plus générale et adaptée à une large gamme de molécules. Il n'est pas nécessaire d'avoir des composés avec des chromophores ou des groupes fonctionnels UV-visibles car le signal thermique est une propriété universelle des réactions de liaison. Dans le même temps, le rapport signal sur bruit est assez favorable, ce qui permet une détermination plus précise des constantes de liaison, même dans des conditions très diluées[11]. Un exemple récent de l'utilisation de cette technique était d'étudier l'affinité de liaison de la membrane protéique entourant Escherichia coli aux cations lipophiles utilisés dans les médicaments dans divers environnements mimétiques membranaires. La motivation de l'étude ci-dessus était que ces membranes rendent les bactéries résistantes à la plupart des composés à base de cation ammonium quaternaire, qui ont des effets antibactériens. Ainsi, une compréhension des phénomènes de liaison permettrait de concevoir des antibiotiques efficaces contre E. coli. Les chercheurs ont maintenu un large excès de ligand par rapport à la protéine pour permettre à la réaction de liaison de se terminer. En utilisant les équations ci-dessus, les chercheurs ont procédé au calcul , , et pour chaque médicament dans des environnements différents. Les données ont indiqué que la stœchiométrie de liaison du médicament avec la membrane était de 1:1 avec une valeur micromolaire de . Les valeurs négatives de , et ont indiqué que le processus était entraîné par l'enthalpie avec une valeur de 8 à 12 kcal/mol pour chaque médicament[12].


![{\displaystyle K_{\text{a}}^{\ominus }={\frac {\{HG\}}{\{H\}\{G\}}}={\frac {[HG]}{[H][G]}}\times \Gamma }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7c1d4e7fbeb2a4cd0a86270abd805fdd2279f3d1)
![{\displaystyle [HG]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/80fdda7af86666fc9f3342541e225ac292bb9a81)
![{\displaystyle [H]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/59d2226487b5eb5f8a607d7233b5825b05775db6)
![{\displaystyle [G]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3b230fd410e2cd9ecc472bb1de122c0b523f561c)

![{\displaystyle K_{\text{a}}={\frac {[HG]}{[H][G]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/54f3e042d0f6f82090d2a9f9b784c57e660ed70b)




![{\displaystyle K={\frac {[HG]}{[H][G]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f0699f3a1a1574661940baea1c8bbfb4a3136447)
![{\displaystyle T_{H}=[H]+K[H][G]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4ef4c10eece3b96f87a168ce59d82e54e4c5d249)
![{\displaystyle T_{G}=[G]+K[H][G]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1246c000c420a8e140e2ef3450c8ed780b7eea5b)


![{\displaystyle [H]=T_{H}-T_{G}+[G]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4cab49660f203c07b5f2b895ab2f8c1545cbbd8c)
![{\displaystyle [HG]=K[H][G]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e88c585a975e89e21c0933648c84b4fdedd50c12)











![{\displaystyle \beta _{pq}={\frac {[H_{p}G_{q}]}{[H]^{p}[G]^{q}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/db509ff939d1eb629ba6b10c11abc7b380a95c76)
![{\displaystyle T_{H}=[H]+\sum p\beta _{pq}[H]^{p}[G]^{q}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e85683a8e3d63267f6160f59ea79b76f9f87ba74)
![{\displaystyle T_{G}=[G]+\sum q\beta _{pq}[H]^{p}[G]^{q}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/515652e9c3e3cd95a67682abf6e924937de71da8)
![{\displaystyle [H_{p}G_{q}]=\beta _{pq}[H]^{p}[G]^{q}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ae16c12c4b85d02e4add18af69d42131945ce0e8)






![{\displaystyle Q={V\Delta H_{0}[H.G]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/05741345df5c805bd41d52801bd5df273f77089c)
![{\displaystyle Q={\frac {V\Delta H_{0}K_{\text{a}}[H_{0}][G]}{1+K_{\text{a}}[G]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3b6ad753a3c264cc520ebf92dc9dcb56f580de32)
![{\displaystyle [H_{0}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b09a9868564ad3a8fc85cbdf4abab3df406316f8)