Chimie des fullerènes
From Wikipedia, the free encyclopedia
La chimie des fullerènes est un domaine de la chimie organique consacré à l'étude des propriétés chimiques des fullerènes[1],[2],[3]. La recherche dans ce domaine est motivée par la nécessité de fonctionnaliser les fullerènes et de modifier leurs propriétés. Par exemple, le fullerène est connu pour être insoluble mais l'ajout d'un groupe adapté peut améliorer sa solubilité. Par l'ajout d'un groupe polymérisable, un polymère du fullerène peut être obtenu. Les fullerènes fonctionnalisés sont divisés en deux catégories : les exofullerènes, avec des substituants à l'extérieur de la cage, et les endofullerènes, avec des molécules piégées dans la cage.
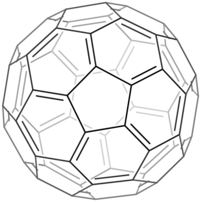
Le fullerène ou C60 a une forme de ballon de football. Sa symétrie appartient au groupe Ih. Il est constitué de 12 pentagones et 20 hexagones. D'après la Caractéristique d'Euler, ces 12 pentagones sont nécessaires pour effectuer la clôture du réseau carboné constitué de n hexagones, et le C60 est le premier fullerène stable car c'est le plus petit possible obéissant à cette règle. Dans cette structure, aucun des pentagones n'entre en contact avec les autres. À la fois le C60 et son dérivé le C70 obéissent à cette règle du pentagone isolé (RPI). L'homologue suivant, le C84, possède 24 isomères RPI dont plusieurs ont été isolés et 51 568 autres isomères non-RPI. Les fullerènes non-RPI n'ont pour l'instant été isolés que sous forme d'endofullerènes tels que le Tb3N@C84 avec deux pentagones fusionnés au sommet d'une cage en forme d’œuf[4]. ou d'exofullerènes avec stabilisation externe tels que le C50Cl10[5]. et apparemment le C60H8[6]. Les fullerènes inférieurs n'obéissent pas à la règle du pentagone isolé (RPI).
En raison de la forme sphérique de la molécule, les atomes de carbone sp2 ne sont pas plans mais déformés, à mi-chemin vers une géométrie moléculaire trigonale plan, ce qui a de lourdes conséquences sur la réactivité. À cela deux raisons. La première, il est estimé que la tension de cycle représente 80 % de l'enthalpie standard de formation. Les atomes de carbone conjugués répondent à l'écart de planéité par un changement dans l'hybridation orbitalaire des orbitales sp2 et des orbitales pi pour former une orbitale sp2.27 avec un renforcement du caractère p. Les lobes p s'étendent plus loin à l'extérieur de la surface qu'à l'intérieur de la sphère, et c'est l'une des raisons pour lesquelles un fullerène est électronégatif. L'autre raison étant que les orbitales pi* vides et basses en énergie ont également un caractère s élevé.
Les doubles liaisons dans les fullerènes ne sont pas toutes les mêmes. Deux groupes peuvent être identifiés: 30 doubles liaisons notées [6,6] connectent deux hexagones et 60 doubles liaisons [5,6] connectent un hexagone et un pentagone. Les liaisons [6,6] sont plus courtes avec un caractère plus prononcé de double liaison, en conséquence un hexagone est souvent représenté comme un cyclohexatriène et un pentagone comme un pentalène ou [5]radialène. En d'autres termes, bien que les atomes de carbone dans les fullerènes soient tous conjugués la superstructure n'est pas un composé "superaromatique". La diffraction des rayons X donne des longueurs de liaison de 139,1 pm pour les liaisons [6,6] et 145,5 pm pour les liaisons [5,6].
Le fullerène C60 possède 60 électrons pi, mais le remplissage de la couche de valence en nécessite 72. Le fullerène est en mesure d'acquérir les électrons manquants par réaction avec un réducteur comme du potassium pour former d'abord le sel K6C60, ce qui correspond à C606− puis le K12C60, ce qui correspond à C6012−. Dans ce composé l'alternance des longueurs de liaison observée avec la molécule de départ a disparu.
Réactivité des fullerènes
Les fullerènes ont tendance à réagir en tant qu'électrophiles. Leur réactivité est augmentée par la suppression de la tension de cycle lorsque les doubles liaisons deviennent saturées. L'élément clé dans ce type de réaction est la quantité de fonctionnalisations, par exemple une monoaddition vs. une polyaddition et, dans le cas de la polyaddition, les relations topologiques entre les fragments ajouté (substituants entassés vs. espacés régulièrement). En conformité avec les règles de l'IUPAC, les termes méthanofullerènes sont utilisés pour indiquer les dérivés du fullerène dont le substituant se referme en cycle (cyclopropane), et fulleroïdes pour ceux dont le substituant est ouvert (méthanoannulènes).
Addition nucléophile
Les fullerènes réagissent en tant qu'électrophiles avec de nombreux nucléophiles pour subir des additions nucléophiles. L'intermédiaire formé (un carbanion) est capturé par un autre électrophile. Des exemples de nucléophiles sont les réactifs de Grignard et les organolithiens. Par exemple, la réaction du C60 avec le chlorure de méthylmagnésium s'arrête quantitativement à la penta-addition avec les groupes méthyles centrés autour d'un anion cyclopentadiényle qui est par la suite protoné. Une autre réaction nucléophile est la réaction de Bingel. Le fullerène réagit avec le chlorobenzène et le chlorure d'aluminium dans une réaction d'alkylation de Friedel et Crafts. Cette hydroarylation forme le produit de l'addition 1,2ː le (Ar-CC-H).
Réactions péricycliques
Les liaisons [6,6] des fullerènes réagissent en tant que diènes ou diénophiles dans les cycloadditions comme la réaction de Diels-Alder. Des cycles à 4 atomes peuvent être obtenus par cycloadditions [2+2] avec par exemple le benzyne[7],[8] Un exemple de cycloaddition 1,3-dipolaire formant un cycle à 5 atomes est la réaction de Prato.
Hydrogénation
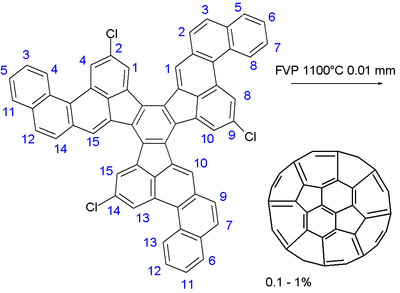
Les fullerènes sont facilement hydrogénés par plusieurs méthodes. Des exemples d'hydrofullerènes sont le C60H18 et le C60H36. Cependant, le C60H60 totalement hydrogéné n'est qu'hypothétique en raison de la forte tension de cycle. Les fullerènes trop hydrogénés ne sont pas stables car la réaction directe des fullerènes avec de l'hydrogène gazeux à haute température provoque une fragmentation de la cage. Lors de l'étape finale de la réaction, la fragmentation résulte en l'effondrement de la structure de la cage accompagnée par la formation d'hydrocarbures aromatiques polycycliques[9].
Oxydation
Bien que plus difficile que sa réduction, l'oxydation du fullerène est possible, par exemple avec de l'oxygène et du tétroxyde d'osmium.
Hydroxylation
Les fullerènes peuvent être hydroxylés en fullerénols ou fullerols. La solubilité dans l'eau dépend du nombre total de groupes hydroxyles qui peuvent y être attachés. Une méthode est de faire réagir le fullerène dans de l'acide sulfurique dilué en présence de nitrate de potassium pour former du C60(OH)15[10],[11] Une autre méthode est la réaction dans de l'hydroxyde de sodium dilué catalysée par l'hydroxyde de tétrabutylammonium, ce qui ajoute entre 24 et 26 groupes hydroxyles au composé[12] L'hydroxylation a également été observée dans une réaction sans solvant avec le mélange NaOH / peroxyde d'hydrogène[13] Le C60(OH)8 a été préparé en utilisant une procédure multi-étapes débutant à partir d'un mélange de peroxyde et de fullerène[14]. Le nombre maximum de groupes hydroxyle qui peuvent être attachés (méthode au peroxyde d'hydrogène) s'élève à 36-40[15].
Addition électrophile
Les fullerènes réagissent aussi dans des additions électrophiles. La réaction avec le brome peut ajouter jusqu'à 24 atomes de brome à la sphère. Le détenteur du record pour l'addition de fluor est le C60F48. Selon des prédictions in silico l'insaisissable C60F60 pourrait avoir certains de ses atomes de fluor en position endo (pointant vers l'intérieur) et pourrait ressembler à un tube plus qu'à une sphère[16].
Rétroadditions
Des protocoles ont été étudiés pour la suppression de substituants via des rétroadditions après que ces substituants aient rempli leur rôle. Des exemples sont la rétroréaction de Bingel et la rétroréaction de Prato.
Addition de Carbènes
Les fullerènes réagissent avec les carbènes pour former des méthanofullerènes[17]. La réaction du fullerène avec le dichlorocarbène (créé par pyrolyse du trichloroacétate de sodium) a été observée pour la première fois en 1993[18]. Une simple addition se fait le long d'une liaison [6,6].
Addition de radicaux
Les fullerènes peuvent être considérés comme des piégeurs de radicaux. Avec un radical alkyle tel que le radical du t-butyle obtenu par thermolyse ou photolyse d'un précurseur approprié, le radical tBuC60 est formé et peut être étudié. L'électron non apparié ne se délocalise pas sur l'ensemble de la sphère, mais il se place au voisinage du substituant tBu.
Les fullerènes en tant que ligands
Le fullerène est un ligand en chimie organométallique. La double liaison [6,6] est déficiente en électrons et forme généralement des liaisons métalliques avec une hapticité η = 2. Des modes de liaisons tels que η = 5 ou η = 6 peuvent être induits par la modification de la sphère de coordination. Le fullerène C60 réagit avec de l'hexacarbonyle de tungstène W(CO)6 pour former le complexe (η2-C60)W(CO)5 dans une solution d'hexane au contact direct de la lumière du soleil[19].
Variantes
Fullerènes à cage ouverte
Une partie de la recherche sur les fullerènes est consacrée aux fameux fullerènes à cage ouverte [20] chez lesquels une ou plusieurs liaisons ont été chimiquement détruites pour ouvrir un orifice[21]. De cette manière, il est possible d'insérer à l'intérieur de petits atomes tels que l'hydrogène, l'hélium ou le lithium. Le premier de ces fullerènes à cage ouverte a été observé en 1995[22] Pour les endofullerènes hydratés l'ouverture, l'insertion de l'hydrogène et la fermeture de l'orifice ont déjà été ̩effectuées.
Hétérofullerènes
Dans les hétérofullerènes au moins un atome de carbone est remplacé par un autre élément[23],[24]. Basées sur la spectroscopie, les substitutions ont été effectuées avec le bore (borafullerènes)[25],[26], l'azote (azafullerènes)[27],[28], l'oxygène[29], l'arsenic, le germanium[30], le phosphore[31], le silicium[32], le fer, le cuivre, le nickel, le rhodium[33]. et l'iridium[34] Les publications sur les hétérofullerènes isolés sont limités à ceux qui contiennent de l'azote[35],[36],[37],[38]. et de l'oxygène[39].
Dimères de fullerènes
Le C60 fullerène se dimérise par cycloaddition [2+2] pour former un C120 en forme d'haltère à l'état solide par mécanochimie (haute vitesse de vibration de fraisage), avec le cyanure de potassium en tant que catalyseur[40]. Le trimère a également été obtenu avec la 4-aminopyridine comme catalyseur (4 % de rendement)[41]. et observé par microscopie à effet tunnel, présentant une forme de monocouche[42].