Psoralène
From Wikipedia, the free encyclopedia
| Psoralène | |

| |
| Identification | |
|---|---|
| Nom UICPA | 7H-furo[3,2-g]chromèn-7-one ou 7H-furo[3,2-g]benzopyran-7-one |
| No CAS | |
| No ECHA | 100.000.581 |
| No CE | 200-639-7 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores |
| Propriétés chimiques | |
| Formule | C11H6O3 [Isomères] |
| Masse molaire[1] | 186,163 5 ± 0,010 1 g/mol C 70,97 %, H 3,25 %, O 25,78 %, |
| Propriétés physiques | |
| T° fusion | 163 à 164 °C[2] |
| Précautions | |
| Directive 67/548/EEC | |
| Écotoxicologie | |
| LogP | 1,67[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
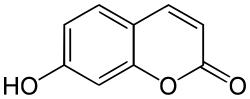
Le psoralène est un composé chimique naturel de la famille des furocoumarines. Sa structure est donc celle des coumarines à laquelle est fusionné un cycle de furane. C'est un dérivé de l'ombelliférone.
Le psoralène est naturellement présent dans les graines de Psoralea corylifolia (babchi), mais aussi dans le figuier commun, le céleri, la berce du Caucase, les arbustes du genre Zanthoxylum, plusieurs espèces de fabacées des genres (Otholobium, Psoralea et coronilla)[3] et en moins forte concentration dans les agrumes, l'aneth, le persil, le panais et les chrysanthèmes (Rutaceae et Apiaceae). Il est très utilisé en PUVA-thérapie (=psoralène+UVA) contre le psoriasis, l'eczéma, le vitiligo, et des lymphomes cutanés de lymphocytes T. Bien que sans danger mortel pour les mammifères, le psoralène doit être utilisé avec précaution car, comme de nombreuses furocoumarines, il est extrêmement toxique pour les poissons. Agent photosensibilisant, il peut toutefois être la cause de cancers de la peau.
Structure

Un isomère du psoralène est l'angélicine.
La structure du psoralène, une coumarine fusionnée avec un cycle de furane, a originellement été déterminée par des réactions de dégradation ; ainsi, il réagit selon les mêmes réactions que le lactone des coumarines, comme l'ouverture du cycle par un alcali pour donner l'acide coumarinique ou un dérivé de l'acide coumarique, et le permanganate de potassium cause l'oxydation du cycle de furane, tandis que d'autres méthodes d'oxydation produisent l'acide furane-2,3-carboxylique.
Synthèse
La synthèse du psoralène est difficile, car l'ombelliférone subit plus facilement une substitution électrophile aromatique en position 8 que sur la position 6 désirée. Le benzofurane lui réagit préférentiellement par le cycle de furane que par le cycle de benzène. Par contre, le 6-hydroxy-2,3-dihydrobenzofurane (6-hydroxycoumarane) peut subir une substitution permettant la synthèse du groupe coumarine par réaction de Gattermann-Koch, suivie d'une condensation de Perkin utilisant de l'anhydride acétique. La synthèse se termine par une déshydrogénation du cycle à 5 atomes pour donner le cycle de furane.

Biosynthèse

Le psoralène est produit à partir des coumarines, en particulier l'ombelliférone par la voie métabolique des furocoumarines linéaires. Cette biosynthèse fait suite à la voie des phénylpropanoïdes (ou du shikimate) produisant l'ombelliférone à partir de la phénylalanine et de la voie du mévalonate produisant le pyrophosphate de diméthylallyle (DMAPP). Ce dernier est d'abord activé, formant un carbocation par clivage du diphosphate. Une fois activé, l'enzyme ombelliférone 6-prényltransférase catalyse la C-alkylation entre le DMAPP et l'ombelliférone sur la position activée, en ortho du phénol, menant à la formation de la déméthylsubérosine. Cette réaction est suivie par une hydroxylation catalysée par l'enzyme marmésine synthase formant la marmésine, suivie d'une seconde hydroxylation avec départ d'acétone catalysée par la psoralène synthase formant le psoralène[4].
