Éthylate de titane
From Wikipedia, the free encyclopedia
| Éthylate de titane | |

| |
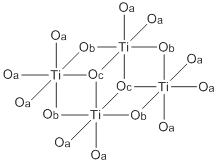
| Structure de l'éthylate de titane | |
| Identification | |
|---|---|
| Nom systématique | éthanolate de titane(IV) |
| No CAS | |
| No ECHA | 100.019.464 |
| No CE | 221-410-8 |
| PubChem | 76524 |
| SMILES | |
| InChI | |
| Apparence | solide blanc cristallisé quand il est pur[1] commercialisé sous forme d'un liquide visqueux jaune clair[2] inflammable[3] |
| Propriétés chimiques | |
| Formule | C8H20O4Ti |
| Masse molaire[4] | 228,109 ± 0,01 g/mol C 42,12 %, H 8,84 %, O 28,06 %, Ti 20,98 %, |
| Propriétés physiques | |
| T° fusion | 40 °C[1] (forme pure solide) −40 °C[3] (forme courante) |
| T° ébullition | 122 °C[3] à 1,33 hPa 150 à 152 °C[3] à 13,3 hPa |
| Solubilité | s'hydrolyse dans l'eau |
| Masse volumique | 1,088 g/cm3[3] à 25 °C |
| Point d’éclair | 42 °C[3] |
| Viscosité dynamique | 50 mPa s[3] à 25 °C |
| Précautions | |
| SGH[3] | |
| H226, H319, P210, P233, P240, P241, P242 et P305+P351+P338 |
|
| Transport[3] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L’éthylate de titane est un composé chimique de formule Ti(OCH2CH3)4, parfois abrégée Ti(OEt)4, où Et représente un groupe éthyle −CH2CH3. Lorsqu'il est parfaitement pur, il se présente sous la forme d'un solide cristallin blanc qui fond vers 40 °C[1], mais est généralement distribué sous la forme d'un liquide visqueux tirant sur le jaune peut-être dû à un état de surfusion[5] ou à une contamination par des produits d'hydrolyse[1]. Le solide présente une structure cristalline appartenant au système monoclinique avec le groupe d'espace C2/c (no 15)[6]. Les molécules Ti(OEt)4 forment des tétramères dans lesquels les atomes de titane sont coordonnés de manière octaédrique, tandis que les atomes d'oxygène des groupes éthylate −OCH2CH3 peuvent se coordonner à un, deux ou trois atomes de titane, avec des liaisons Ti−O de longueur variable selon ces trois cas et formant deux types de centres Ti(IV) selon la géométrie des groupes éthylate coordonnés[6]. Il existe également des structures trimériques en phase liquide et en solution[1],[7],[8],[9].
On peut obtenir l'éthylate de titane en traitant le tétrachlorure de titane TiCl4 avec de l'éthanol EtOH en présence d'une amine[10], telle que la triéthylamine Et3N :
L'éthylate s'hydrolyse dans l'eau en donnant de l'acide titanique H4TiO4 et est soluble dans le toluène et l'acétone.