KLK6
From Wikipedia, the free encyclopedia
KLK6(カリクレイン6、kallikrein-6)は、ヒトではKLK6遺伝子にコードされるタンパク質である[5][6][7][8]。KLK6は、ニューロシン(neurosin)、protease M、hK6、zymeといった名称でも知られる。16残基のシグナル配列、5残基の活性化ペプチドを含む244アミノ酸のポリペプチドとして合成され、223アミノ酸の成熟型へとプロセシングされる[9]。

機能
カリクレインは多様な生理機能を有するセリンプロテアーゼのグループである。多くのカリクレインが発がんに関与しており、その一部はがんやその他の疾患のバイオマーカーとなりうることを示唆するエビデンスが蓄積している。KLK6遺伝子にコードされているプレプロタンパク質は、切断されて成熟型プロテアーゼとなる。このプロテアーゼの発現はステロイドホルモンによって調節されており、またヒトの複数種のがんや乾癬患者の血清で上昇している可能性がある。KLK6はアミロイド前駆体タンパク質やα-シヌクレインの切断に関与している可能性があり、そのためアルツハイマー病やパーキンソン病と関連している可能性が示唆されている。KLK6遺伝子は19番染色体上のカリクレイン遺伝子クラスター内に位置している[8]。
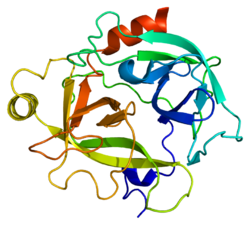
構造
KLK6の二次構造は、13本のβストランド、2本のαヘリックス、2個の310ヘリックス、8か所のループ領域から構成される。アミノ酸配列の面では、ラットのMyelencephalon-Specific Protease(MSP)[10]と最も類似している。MSPとKLK6はどちらもアルギニン残基の後のペプチド結合を標的とし、また自身のタンパク質内のアルギニンに対する自己切断を行う[11]。
構造の面では、KLK6はウシトリプシンと類似している。基質結合部位近傍のループは短く、結合部位から離れるように位置しており、S2、S3部位の形成にはあまり寄与していないようである。S1部位にはアスパラギン酸、ヒスチジン、セリンの触媒三残基に加えて189–195、214–220、224–228番残基が位置している[12]。
病理
α-シヌクレインの蓄積は、レビー小体型認知症、パーキンソン病、多系統萎縮症の患者に広くみられる。α-シヌクレインの分解を担うタンパク質の同定のため、プロテアーゼ阻害剤を用いた探索が行われている。さまざまなセリンプロテアーゼ阻害剤(アプロチニン、PMSF、ロイペプチン、AEBSF)が分解経路に大きな影響を及ぼすことから、α-シヌクレインの分解にセリンプロテアーゼが必要であることが示唆されている。カリクレイン阻害剤も用量依存的に分解を阻害し、また精製されたカリクレインがα-シヌクレインに対する分解活性を有することがin vitroで示されている[13]。
KLK6はこうした疾患の防止に寄与している一方、悪性腫瘍細胞の拡散にも寄与している可能性がある。KLK6は分解酵素として、正常細胞や悪性細胞の双方の細胞外マトリックスを分解する能力を有し、遊走能やシグナル伝達能力を高めている可能性がある。KLK6はフィブロネクチン、ラミニン、ビトロネクチン、コラーゲンなどの細胞外マトリックスタンパク質に対する分解活性を有し、またKLK6中和抗体によって処理された腫瘍細胞は遊走能が低下する[14]。
機構

KLK6はAsp102、His57、Ser195が触媒三残基を形成し、N末端側にアルギニン残基が位置するペプチド結合を特異的に加水分解する[15]。他のセリンプロテアーゼと類似した触媒機構を有すると考えられている[16]。
- ヒスチジン残基がセリン残基を脱プロトン化する
- セリン残基がアミド結合の代替となる
- プロトン化ヒスチジン残基によってアミンがより良い脱離基となり、オキシアニオンが崩壊してエステルが形成される
- 水分子がエステル結合を切断し、セリン残基が脱離する