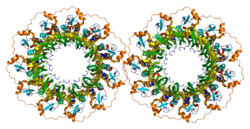
RAD52
From Wikipedia, the free encyclopedia
RAD52は、ヒトではRAD52遺伝子によってコードされるタンパク質である[5][6]。

機能
DNA組換え修復における役割
RAD52は、出芽酵母と哺乳類細胞(マウスとヒト)の双方において、相同組換え修復(HRR)におけるRAD51の機能を媒介する。しかしながら、RAD52のHRRにおける機能は、酵母とヒトでは異なる。出芽酵母ではRad52タンパク質は単独で作用し、組換えの対合前の段階で既にRPAで覆われた一本鎖DNAへRad51タンパク質をロードする役割を果たす[7][8]。
一方マウスとヒトでは、主にBRCA2が一本鎖DNA上でのRAD51の規則的な組み立てを媒介し、相同鎖の対合と鎖の侵入(strand invasion)の活性を有する形態が形成される[9]。また、BRCA2はRAD51のdsDNAへの結合を低下させ、またssDNAからの解離を防ぐ[9]。さらに、RAD51の4つのパラログ、RAD51B(RAD51L1)、RAD51C(RAD51L2)、RAD51D(RAD51L3)、XRCC2はBCDX2複合体と呼ばれる複合体を形成する。この複合体はRAD51の損傷部位へのリクルートと安定化に関与し[10]、RAD51ヌクレオタンパク質フィラメントの組み立てまたは安定性を促進する作用を果たしているようである。しかしながら、BRCA2に変異が存在する場合には、ヒトのRAD52は一本鎖DNA上でのRAD51の組み立てを媒介することができ、より低効率であるものの、相同組換えによるDNA修復におけるBRCA2の代替として機能することができる[11]。
さらに、ヒトのRAD52はERCC1とともに、エラーが起こりやすい相同組換え経路であるSSA(single-strand annealing)経路を促進する[12]。この修復経路はエラーが起こりやすいものの、それ以外の方法では修復できないDNA損傷を抱えた細胞の生存には必要である可能性がある。
ヒトのRAD52は、細胞周期のG0/G1期の活発な転写部位でのDNA二本鎖切断修復に重要な役割を果たす。こうした二本鎖切断の修復においては、RAD52に依存した、RNA鋳型を用いた組換え機構が利用されているようである[13]。ERCC6遺伝子にコードされるコケイン症候群Bタンパク質(CSB)は活発な転写部位の二本鎖切断に局在し、続いてRAD51、RAD51CとRAD52が新たに合成されたRNAを鋳型として相同組換え修復を行う[13]。
miRNAとがんのリスク
mRNAの3' UTRには、転写後段階でのRNAサイレンシングを引き起こす調節配列が含まれていることが多い。こうした3' UTRには多くの場合、miRNAの結合部位が含まれている。miRNAは3' UTR内の特定の部位に結合することで、翻訳の阻害または転写産物の分解によってさまざまなmRNAからの遺伝子発現を減少させる。
miRNAはヒトゲノム中のタンパク質コード遺伝子の60%以上の発現を調節しているようである[14]。そうしたmiRNAの1つ、miR-270はRAD52を抑制する[15]。miR-210は大部分の固形腫瘍でアップレギュレーションされており、臨床転帰に負の影響を与える[16]。
RAD52のmRNAの3' UTRには、let-7の結合部位も存在する。let-7の結合を減少させるSNP(rs7963551)を持つ女性は、RAD52の発現が上昇している可能性が高い(このことは肝臓で示されている[17])。このSNPを持つ女性は乳がんのリスクが低いことが示されている(オッズ比[OR] 0.84、95%信頼区間[CI] 0.75–0.95)[18]。
漢族では、このSNPが神経膠腫のリスクを低下させることが示されている。RAD52 rs7963551遺伝子型と関係した神経膠腫のリスクは42歳以上の場合OR 0.44、41歳以下の場合OR 0.58である[19]。
中国人集団では、RAD52 rs7963551 CC遺伝子型(上述したものと同じ)の肝細胞がんのリスクはAA遺伝子型と比較して有意に低い。また、44種類の正常なヒト肝組織試料を解析した結果、rs7963551 SNPを持つヒトの試料ではRAD52のmRNAの発現が有意に高かった[17]。
このように、RAD52の発現の増加はさまざまながんに対する保護機能となっている。
RAD52のmRNA中のmiRNA結合部位の変化とがん感受性への影響を調べる他の研究も行われている[20]。そこでは、高頻度で変化している2つのmiRNA結合部位が結腸がんのリスクに影響していることが発見された。rs1051669 SNPをホモ接合型またはヘテロ接合型で持っている場合、結腸がんのリスクが高まる(ホモ接合型: OR 1.78, 95% CI 1.13–2.80, p = 0.01; ヘテロ接合型: OR 1.72, 95% CI 1.10–2.692, p = 0.02)。他のSNP(rs11571475)をヘテロ接合型で保有している場合、結腸がんのリスクは低くなる(OR 0.76, 95% CI 0.58–1.00, p = 0.05)。調査が行われた相同組換え修復経路に関与する遺伝子21種類と非相同末端結合経路に関与する遺伝子7種類のうち、評価可能な頻度で変化し、かつ結腸がんのリスクに影響を与えるmiRNA結合部位のSNPが観察されたのは、RAD52の2か所とMRE11Aの1か所のみであった。
DNA損傷はがんの主要な根本要因であるようであり[21]、多くの種類のがんの根底にはDNA修復の欠乏があるようである[22]。DNA修復が欠乏している場合、DNA損傷は蓄積する傾向がある。こうした過剰なDNA損傷は、DNA複製時に損傷乗り越え合成(translesion synthesis)が行われることでエラーの増加をもたらしている可能性がある。また、過剰なDNA損傷はDNA修復時のエラーに伴うエピジェネティックな変化を増加させている可能性もあり[23][24]、こうした変異やエピジェネティックな変化ががんを生じさせている可能性がある。miRNAの結合の変化によるRAD52を介したDNA修復の頻繁な増加または欠乏は、乳がん、脳腫瘍、肝臓がん、大腸がんの予防または進行のいずれかに寄与している可能性が高い。
相互作用
RAD52はRAD51と相互作用することが示されている[25]。
遺伝子内相補性
1つの遺伝子にコードされるポリペプチドが複数コピー集まって凝集体を形成するとき、こうしたタンパク質構造はマルチマー(multimer)と呼ばれる。特定の遺伝子の2つの異なる変異体アレルから産生されるポリペプチドによってマルチマーが形成される場合、こうした混合型マルチマーは各変異体アレル単独から形成される非混合型マルチマーよりも高い機能的活性を示す可能性がある。この現象は遺伝子内相補性(intragenic complementation)と呼ばれる。出芽酵母では、C末端短縮型タンパク質を発現するRAD52変異体アレルが他のミスセンス変異体アレルを相補することが発見されている[26]。こうした遺伝子内相補性の存在は、RAD52タンパク質が単量体間の協同的相互作用を可能にするようなマルチマー構造を持つことを示唆している。