Dehalogenimonas
From Wikipedia, the free encyclopedia
Dehalogenimonas ist eine Gattung von Bakterien. Die Arten sind dazu in der Lage, chlorierte und bromierte Alkane abzubauen und dadurch Energie zu gewinnen. Sie führen also eine Reduktive Dehalogenierung, was auch als Organohalogenid-Atmung bezeichnet wird, durch. Zum Beispiel bildet es aus 1,2-Dichlorethan das Alken Ethen, zwei Chlorwasserstoff-Moleküle und ATP.[1][2]

| Dehalogenimonas | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

Dehalogenimonas alkenigignens Stamm IP3-3T | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Dehalogenimonas | ||||||||||||
| Moe 2009 |
Die Arten wurden u. a. aus kontaminiertem Grundwasser, Boden und Weintraubentrester isoliert. Die Gattung zählt zu der Familie Dehalococcoidaceae innerhalb der Abteilung Grünen Nichtschwefelbakterien (Chloroflexota). Bakterien, die chlorierte Alkane abbauen bilden eine relativ kleine Gruppe, die taxonomisch sehr vielfältig ist. Ein anderes Beispiel ist die Gattung Dehalococcoides, die zu derselben Familie wie Dehalogenimonas gehört, sowie Desulfuromonas und Sulfurospirillum.[1]
Merkmale
Die Zellen von Dehalogenimonas sind unregelmäßig geformte Kokken. Endosporen werden nicht gebildet. Der Gram-Test fällt negativ aus, d. h. die Arten besitzen eine äußere Hülle bestehend aus einer inneren Membran, einer dünnen Peptidoglykan-Schicht und einer äußeren Membran. Die Arten sind unbeweglich. Die Zellen von Dehalogenimonas alkenigignens und D. lykanthroporepellens sind relativ klein, mit einem Durchmesser von 0,3–1,1 µm.
Arten der Gattung Dehalogenimonas bilden selbst nach längerer Inkubation (2 Monate) auf mit Agar oder Gellangummi verfestigten Nährmedien keine sichtbaren Kolonien und in Flüssigkultur gezüchtete Kulturen weisen keine hohe Trübung auf. Maximale Zellkonzentrationen in der Größenordnung von 107 Zellen pro ml wurden routinemäßig bei Batch-Kultivierung unter Laborbedingungen beobachtet.[1]
Stoffwechsel und Wachstum

Dehalogenimonas-Arten leben strikt anaerob, tolerieren also keinen Sauerstoff. Sie sind mesophil mit einem Temperaturoptimum von etwa 30 °C. Sie sind neutrophil, mit einem pH-Optimum von etwa 7,0. Die Arten sind chemotroph und nutzen halogenierte organische Verbindungen als Elektronenakzeptoren sowie Wasserstoff (H2) oder Formiat als Elektronendonatoren. Sie zählen somit zu den Organohalogenid-Atmer. Diese Bakterien „atmen“ also halogenierte organische Moleküle (Organohalogenide oder Organohalogene genannt) ähnlich wie der Mensch Sauerstoff einatmet. Biochemisch gesehen nutzen Organohalogenid-Atmer Organohalogenide als terminale Elektronenakzeptoren in einer Atmungskette, die an den gerichteten Protonentransport durch die Zellmembran und die Energieerhaltung gekoppelt ist. Die benötigten Elektronen stammen von externen Elektronendonatoren wie molekularem Wasserstoff oder anderen oxidierbaren Verbindungen. Dabei werden die halogenierte Verbindungen reduziert, indem die Halogensubstituenten abgespalten und gleichzeitig Elektronen hinzugefügt werden. Die reduktive Dehalogenierung wird durch membranassozierte Enzyme, den Dehalogenasen, katalysiert. Hierbei wird mit Hilfe einer ATPase ATP erzeugt. Die entfernten Halogensubstituenten werden als Anionen freigesetzt.[3][4]
Chlorierte und bromierte organische Verbindungen sind die einzigen, bekannten terminalen Elektronenakzeptoren, die von Mitgliedern der Gattung Dehalogenimonas genutzt werden.[1]

Man unterscheidet zwei Arten der Organohalogenid-Atmung: Hydrogenolyse und Dihalogeneliminierung. Bei der Hydrogenolyse entsteht pro zwei Mol H2 nur ein Mol HX (wobei X für Chlor (Cl), Brom (Br), Flur (F) oder Iod (I) steht), bei der Dihalogeneliminierung hingegen zwei Mol HX pro zwei Mol H2. Die Dihalogeneliminierung erfordert zwei benachbarte Halogene und führt zur Bildung einer ungesättigten C=C-Bindung. Aufgrund der Elektronenkonfiguration des aromatischen Rings findet bei aromatischen Verbindungen keine Dihalogeneliminierung statt.[5] Bei der Dihalogeneliminierung beträgt die Änderung des Wertes der freien Gibbs-Energie (ΔG o′) für die Bildung von HCl −171,2 kJ/mol (dies gilt bei einem pH-Wert von 7). Alle bisher bei den Arten Dehalogenimonas lykanthroporepellens und D. alkenigignens festgestellten reduktiven Dechlorierungsreaktionen scheinen einen ausschließlich auf Dihalogenelimination basierenden Reaktionsmechanismus zu beinhalten, bei dem gleichzeitig zwei Halogene aus benachbarten Kohlenstoffatomen entfernt werden und eine Kohlenstoff-Kohlenstoff-Doppelbindung entsteht.[2] Der Stamm Dehalogenimonas sp. WBC-2 ist dazu in der Lage, trans-Dichloroethen zu Vinylchlorid umzuwandeln und führt somit die Hydrogenolyse durch.[6]
So wird 1,2-Dichlorethan zu Ethen umgewandelt. Die Verbindung 1,2-Dichlorpropan wird zu Propen und 1,1,2-Trichlorethan zu Vinylchlorid (VC) umgewandelt. 1,1,2,2-Tetrachlorethan wird in Dichlorethen, die Verbindung 1,2,3-Trichlorpropan in Allylchlorid (3-Chlor-1-propen) umgewandelt, eine instabile Verbindung, die abiotisch mit Wasser zu Allylalkohol reagieren kann. Sind Sulfid oder Cystein vorhanden, können aus dem reaktiven Zwischenprodukt Allylchlorid weitere Produkte wie S-Allylcystein, Diallylsulfid, Diallyldisulfid, Allylmercaptan und Allylmethylsulfid entstehen.
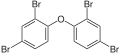
Des Weiteren kann Dehalogenimonas auch die Bromverbindung 2,2’,4,4’-Tetrabromdiphenylether (BDE-47) nutzen.[7][8]
Wasserstoff (H2) und Formiat dienen Dehalogenimonas-Arten als Elektronendonatoren. Dies unterscheidet sie von der verwandten Gattung Dehalococcoides, die ausschließlich H2 nutzt. Die Gattung Dehalococcoides zählt zu der gleichen Familie wie Dehalogenimonas, den Dehalococcoidaceae. Während die Erstbeschreibung von D. alkenigignens darauf hindeutete, dass Formiat nicht als Elektronendonator verwendet wird, bestätigten spätere Untersuchungen, dass D. alkenigignens, D. formicexedens und D. lykanthroporepellens Formiat verwerten können. Das Wachstum von Dehalogenimonas-Arten mit Formiat oder mit Wasserstoff als Elektronendonatoren sind vergleichbar. Arten von Dehalogenimonas zeigen die schnellste Dechlorierung im mesophilen Temperaturbereich mit optimalem Wachstum bei etwa 30 °C. Die Temperaturbereiche für die Dechlorierung und die pH- und Salzgehaltsbereiche für die Dechlorierung variieren leicht zwischen den Arten.[1]
Es folgt eine Tabelle mit Merkmalen einiger Arten:[1]
| Eigenschaften | D. alkenigignens | D. formicexedens | D. lykanthroporepellens | D. etheniformans |
|---|---|---|---|---|
| Quelle | Kontaminiertes Grundwasser | Kontaminiertes Grundwasser | Kontaminiertes Grundwasser | Traubentrester |
| Zellmorphologie | Unregelmäßige Kokken | Unregelmäßige Kokken | Unregelmäßige Kokken | keine Angabe |
| Wachstumstemperatur (°C) | 18–42 | 20–37 | 20–37 | 20–30 |
| Wachstums-pH-Bereich | 6.0–8.0 | 5.5–7.5 | 6.0–8.0 | keine Angabe |
| Entchlorung mit NaCl 1,1 % (w/v) | Ja | Nein | Ja | keine Angabe |
| Größe vom Genom des Typstamms in Megabasenpaare | 1.85 | 2.09 | 1.69 | 2.02 |
| DNA-G+C-Gehalt (mol%) | 55.9 | 54.0 | 55.0 | 52.0 |
| tRNA-Gene | 47 | 49 | 47 | 47 |
Ökologie
Drei Arten, Dehalogenimonas alkenigignens, D. lykanthroporepellens und D. formicexedens, wurden aus mit chlorierten Lösungsmitteln kontaminiertem Grundwasser im Südosten von Louisiana (USA) isoliert.[9][10][11] Der Fundort der zuerst beschriebene Art, Dehalogenimonas lykanthroporepellens, war mit hohen Konzentrationen chlorierter Alkane und Alkene gekennzeichnet. An dem Standort, an dem der Organismus erstmals isoliert wurde, wurden in der Vergangenheit verschiedene flüssige Abfälle aus der chemischen Industrie direkt in unbefestigte Erdbecken eingeleitet. Die Schadstoffe verbleiben im Untergrund als dichte, nichtwässrige Flüssigkeiten.[12] Die Untersuchung zielte darauf hin, Bakterien zu identifizieren, die die hohen Lösungsmittelkonzentrationen an diesem Standort tolerieren.[2] Dehalogenimonas alkenigignens wurde später in einem anderen Bereich desselben Standorts gefunden, allerdings in einer kontaminierten Grundwasserbereich mit deutlich geringeren Konzentrationen an chlorierten Schadstoffen.[13]
Kultivierungsunabhängige, auf dem 16S-rRNA-Gen basierende Methoden zeigten, dass Arten von Dehalogenimonas im Grundwasser in der Umgebung, in der die Stämme isoliert wurden, weit verbreitet waren und in einigen Fällen einen hohen Anteil der Bakteriengemeinschaft ausmachten. In einer Untersuchung von mehr als 1000 Grundwasserproben, die an 111 mit chlorierten Lösungsmitteln kontaminierten Standorten in den Vereinigten Staaten und Australien entnommen wurden, wurde Dehalogenimonas mit kultivierungsunabhängigen Methoden auf Basis des 16S-rRNA-Gens mit einer hohen Häufigkeit (80,6 % der Proben) nachgewiesen, die Gattung kommt also häufig in kontaminierten Umgebungen vor.[14] Aufgrund der begrenzten Auswahl an bekannten Elektronendonatoren H2 und Formiat wachsen Mitglieder der Gattung Dehalogenimonas wahrscheinlich in syntrophen Beziehungen mit anderen Bakterien in der Umwelt. Kultivierungsunabhängige, auf dem 16S-rRNA-Gen basierende Methoden zeigten, dass Dehalogenimonas spp. nach der Injektion des fermentierbaren Substrats Melasse in den Untergrund an Häufigkeit zunahmen.[1][15]
Die verwandte Gattung Dehalococcoides wurde zusammen mit Dehalogenimonas in 849 Proben (72,4 % der Gesamtzahl) nachgewiesen, die räumliche Verbreitung dieser beiden Gattungen überschneidet sich also. Kultivierungsunabhängige, auf dem 16S-rRNA-Gen basierende Methoden haben ebenfalls das Vorhandensein von Dehalogenimonas in Gebieten nachgewiesen, in denen chlorierte Lösungsmittel als Flüssigkeiten mit einer größeren Dichte als Wasser (DNAPLs) im Untergrund vorhanden sind.[1][16]
Die Bildung von niedriger chlorierten Ethenverbindungen, insbesondere Vinylchlorid, ist aus ökologischer Sicht als gefährlich zu betrachten. Allerdings kommen Dehalogenimonas- Stämme oft zusammen mit der dehalogenierenden Gattung Dehalococcoides vor. Die Stämme von Dehalococcoides können Dichlorethen und Vinylchlorid dann vollständige abbauen.[2]
D. lykanthroporepellens war die erste Spezies, die in Reinkultur 1,2,3-Trichlorpropan reduktiv dehalogenieren konnte. Das direkte Produkt ist hier Allylchlorid (3-Chlor-1-Propen), eine relativ instabile Verbindung, die rasch abiotisch hydrolysiert werden kann und zudem mit Sulfiden und Cystein reagiert, die als Reduktionsmittel im Nährmedium vorhanden waren. Letztendlich führte dies zur Bildung verschiedener nichtchlorierter Endprodukte, darunter Diallylsulfid, Diallyldisulfid, Allylmercaptan und Allylmethylsulfid. Diese Endprodukte weisen ein stechendes, knoblauchartiges Aroma auf und gaben der Art ihren Namen, der sich aus dem Lateinischen und Griechischen mit „für Werwölfe abstoßend“ übersetzen lässt. Bei Kultivierung in Medien ohne Sulfid als Reduktionsmittel ist Allylalkohol, der durch abiotische Hydrolyse des Dihalogeneliminierungsprodukts Allylchlorid entsteht, das Hauptprodukt der 1,2,3-Trichlorpropan-Dechlorierung durch Dehalogenimonas alkenigignens und D. lykanthroporepellens.[2]
„Candidatus Dehalogenimonas loeffleri“ dechloriert unter Bedingungen mit hohem Salzgehalt (z. B. 5,1 % NaCl) eine 1,2-Dichlorethan (1,2-DCA). Es ist die erste beschriebene Art von Dehlaogenimonas, die solche hohen Salzgehalte toleriert. Der Stamm wurde aus Sedimenten des Mündungsgebiets, die im Juni 2018 an der Mündung des Flusses Wuli in das Bohai-Meer in der Stadt Huludao in der Provinz Liaoning (40°44′44″N, 120°59′11″E) entnommen wurden.[17]
In der GenBank-Datenbank finden sich eine Vielzahl von 16S-rRNA-Gensequenzen von nicht kultivierten Bakterien, die eine Sequenzidentität von >95 % mit Typstämmen von Dehalogenimonas, aber nur eine Sequenzidentität von ∼90 % mit Dehalococcoides-Stämmen aufweisen. Diese stammen aus geografischen Regionen in Nordamerika, Europa und Asien. Ein Großteil dieser Sequenzen stammt aus kontaminierten Umgebungen oder dechlorierenden Anreicherungskulturen.[1]

Die bakterielle Dehalorespiration ist der wichtigste ökologische Prozess zur Entgiftung von chlorierten Kohlenwasserstoffen unter Sauerstoffausschluss, also unter anaeroben Bedingungen. Bekannte dehalorespirierenden Bakterien gehören zu den Firmicutes (Desulfitobacterium und Dehalobacter), den Proteobacteria (Desulfomonile, Desulfuromonas, Sulfurospirillum) und den Chloroflexi (Dehalococcoides und Dehalogenimonas). Sulfurispirillum wurde früher unter den Namen Dehalospirillum geführt. Auch ein Vertreter der Die Art Anaeromyxobacter dehalogenans, ein Vertreter der Myxococcales, zählt zu den chloratmenden Mikroorganismen.[19]
Genetik
Für die Typusstämme der drei Dehalogenimonas-Arten D. alkenigignens, D. formicexedens und D. lykanthroporepellens liegen Genomsequenzen vor. Die Genome sind relativ groß (1,69 Megabasenpaare für D. lykanthroporepellens Stamm BL-DC-9 und 2,09 Mb für D. formicexedens Stamm NSZ-14) und weisen einen höheren GC-Gehalt auf als die der verwandten Gattung Dehalococcoides. Die Genome der drei Dehalogenimonas-Typstämme enthalten jeweils einen einzigen Genlocus der großen Untereinheit der Ribosomen (23S-5S) und einen einzigen, entfernt gelegenen kleinen Untereinheit-rRNA-Locus (16S).
Die Anzahl der tRNA-Gene reicht bei den drei Arten von 47 bis 49 und umfasst die Gene, die für alle 20 Standardaminosäuren sowie für die weniger verbreitete Aminosäure Selenocystein kodieren. Ein Operon (selCDAB), das mit der Selenocystein-Synthese und der Insertion der Selenocystein-Synthese assoziiert ist, ist ebenfalls in jedem der Typstamm-Genome vorhanden. In Übereinstimmung mit der experimentellen Beobachtung, dass Arten von Dehalogenimonas Formiat als Elektronendonor verwenden können, enthalten die drei Dehalogenimonas-Genome Gene, die vermutlich selenocysteinhaltige Proteine kodieren, darunter Dehydrogenasen für Formiat.
Alle Genome enthalten mehrere reduktive Dehalogenase-Gene (rdhA), von denen viele keine zugehörigen Membrananker-Gene (rdhB) und weniger Transkriptionsregulatoren als in Dehalococcoides aufweisen. Eine große Mehrheit der rdhA-Gene in Genomsequenzen aus der verwandten Gattung Dehalococcoides ist mit MarR- oder Zweikomponenten-System-Transkriptionsregulatoren assoziiert. Im Gegensatz dazu sind solche Transkriptionsregulatoren nur mit einer Minderheit der rdhA-Gene in Dehalogenimonas-Stämmen assoziiert. Experimente mit reverser Transkriptase-Polymerase-Kettenreaktion (PCR) zeigten, dass der Typstamm von D. lykanthroporepellens während der Dechlorierung von 1,2-Dichlorethan, 1,2-Dichlorpropan und 1,2,3-Trichlorpropan gleichzeitig eine große Anzahl von rdhA-Genen transkribiert.
Aus Metagenomen von Mischkulturen, die reduktive Dehalogenierung durchführen, wurden drei weitere Dehalogenimonas-verwandte Genome rekonstruiert. Ein Genom ist in seiner 16S-rRNA-Sequenz nahezu identisch mit D. formicexedens, unterscheidet sich jedoch stark auf der Ebene des gesamten Genoms, sodass es als neue Spezies „Candidatus Dehalogenimonas etheniformans“ vorgeschlagen wurde. Im Jahr 2023 wurde dann die Candidatus-Art zur vollständig beschriebenen Art Dehalogenimonas etheniformans transferiert.[20][21] Diese Art ist dazu Fähig, die chlorierten Ethene Trichlorethen (TCE), 1,2-Dichlorethen (cDCE) und 1,1-Dichlorethen (DCE) und Vinylchlorid CVC) als Elektronenakzeptoren zu verwerten. Diese Verbindungen werden vom D. formicexedens-Typstamm nicht dechloriert. Der G+C-Gehalt von 52,0 mol% der vorläufigen Genomsequenz von "Candidatus D. etheniformans" ist ebenfalls deutlich niedriger als der G+C-Gehalt von 54,0 mol% bei D. formicexedens NSZ-14.
Ein zweites Genom (GenBank-Zugangsnummer QEFQ00000000) stimmt in der 16S-rRNA-Sequenz mit D. alkenigignens überein, hat jedoch einen etwas höheren GC-Gehalt und ein kleineres Genom (1,65 gegenüber 1,85 Mb). Ein drittes Genom von Dehalogenimonas sp. WBC-2 (GenBank-Zugangsnummer CP011392) weist eine geringere 16S-Identität und einen geringeren GC-Gehalt auf, wodurch seine Klassifizierung weniger sicher ist. Obwohl die moderate Identität der 16S-rRNA-Gensequenz und der deutlich niedrigere GC-Gehalt des Genoms von 49,2 % die Authentizität als Dehalogenimonas sp. weniger sicher machen, stützt die Analyse verketteter Proteinsequenzen in der Genome Taxonomy Database (GTDB) die Klassifizierung als Dehalogenimonas sp.[22] Alle drei unkultivierten Genome weisen wichtige genomische Merkmale auf, die auch bei bekannten Dehalogenimonas zu finden sind: mehrere reduktive Dehalogenase-Gene (rdhA), oft ohne rdhB-Membrananker-Gene, separat gelegene Einzelkopien von rRNA-Genen und Gene für die Selenocystein-Synthese und -Insertion.[1][23]
Die im Jahr 2024 beschriebene Art “Candidatus Dehalogenimonas loeffleri” Stamm W zeigt ein 1,77 Mb (1,772.240 bp) langes Chromosom mit einem G+C-Gehalt von 52,5 % und umfasst 1.763 proteinkodierende Sequenzen, darunter 28 Gene, die reduktive Dehalogenasen kodieren.[17]
Nur wenige reduktive Dehalogenasen aus Dehalogenimonas wurden experimentell charakterisiert. Ein Enzym, DcpA, wandelt 1,2-Dichlorpropan zu Propen um und wurde erstmals in D. lykanthroporepellens identifiziert, wobei homologe Gene auch in D. alkenigignens und D. formicexedens vorhanden sind. Ein weiteres Enzym, die trans-1,2-Dichlorethen-reduktive Dehalogenase TdrA, das trans-1,2-Dichlorethen reduziert, wurde in Dehalogenimonas sp. WBC-2 identifiziert.[1]
Systematik
Dehalogenimonas wurde mit D. lykanthroporepellens als Typusart im Jahr 2009 zuerst beschrieben. Sie zählt zu der Familie Dehalococcoidaceae innerhalb der Ordnung Dehalococcoidales der Klasse Dehalococcoidia. Die Klasse zählt zu dem Phylum Chloroflexota innerhalb des Reiches Bacillati. Zu der Familie zählt neben Dehalogenimonas noch die Gattung Dehalococcoides die im Jahr 2013 von Frank E. Löffler und Mitarbeitern beschrieben wurde.
Mit einer Ähnlichkeit der 16S-rRNA-Gensequenzen von nur etwa 90 % lassen sich Arten von Dehalogenimonas durch Sequenzierung leicht von der verwandten Gattung Dehalococcoides unterscheiden. Der GC-Gehalt der DNA von 49,2–56,3 mol% in den Genomen von Dehalogenimonas ist höher als der für die verwandte Gattung Dehalococcoides bestimmte Wert von 47,0–48,9 mol%. Auch zelluläre Fettsäuren dienen als Grundlage für die Unterscheidung, wobei Dehalogenimonas-Stämme einen hohen Anteil an einfach ungesättigten Fettsäuren (z. B. C18:1ω9c und C16:1 ω9c) und Dehalococcoides-Stämme einen hohen Anteil an verzweigten, gesättigten Fettsäuren (z. B. 10-Methyl-C16:0) enthalten.[1][24][25]
Es folgt eine Liste der Arten (Stand Februar 2026):[26]
- Dehalogenimonas alkenigignens Bowman et al. 2013
- Dehalogenimonas etheniformans Cui et al. 2023
- Dehalogenimonas formicexedens Key et al. 2017
- ''Candidatus'' Dehalogenimonas loeffleri Wang et al. 2024
- Dehalogenimonas lykanthroporepellens Moe et al. 2009