Prostatakrebs
bösartige Tumorerkrankung, die vom Drüsengewebe der Vorsteherdrüse (Prostata) ausgeht
From Wikipedia, the free encyclopedia
Der Prostatakrebs oder das Prostatakarzinom (PCa) ist eine bösartige Tumorerkrankung und geht vom Drüsengewebe der Vorsteherdrüse (Prostata) aus. In Deutschland ist das Prostatakarzinom beim Mann der häufigste bösartige Tumor und nach Lungenkrebs die häufigste Tumorlokalisation aller Krebssterbefälle.[1]
| Klassifikation nach ICD-10 | |
|---|---|
| C61 | Bösartige Neubildung der Prostata |
| ICD-10 online (WHO-Version 2019) | |
| Klassifikation nach ICD-11 | |
|---|---|
| 2C82 | Bösartige Neubildungen der Prostata |
| 2C82.0 | Adenokarzinom der Prostata |
| 2C82.Y | Sonstige näher bezeichnete bösartige Neubildungen der Prostata |
| 2C82.Z | Bösartige Neubildungen der Prostata, nicht näher bezeichnet |
| ICD-11: Englisch • Deutsch (Vorabversion) | |
Die Erkrankung ist im Frühstadium symptomlos. Im fortgeschrittenen Stadium können Beschwerden wie Blasenentleerungsstörungen, Knochenschmerzen und später Gewichtsverlust und Blutarmut auftreten. Wird die Diagnose erst gestellt, wenn bereits Symptome aufgetreten sind, hat häufig schon eine Metastasierung stattgefunden, vorrangig in die lokalen Lymphknoten oder in das Skelett (Knochenmetastasen).
Eine Behandlung mit Aussicht auf Heilung ist nur möglich, wenn das entartete Gewebe die Organgrenzen noch nicht überschritten hat und keine Metastasen vorliegen. Da es in der Regel erst bei fortgeschrittener Erkrankung zu Beschwerden kommt, wird in Deutschland eine regelmäßige Früherkennungsuntersuchung für Männer über 45 Jahren (ab dem 41. Lebensjahr für Männer mit positiver Familienanamnese) angeboten, um die Krebsdiagnose möglichst früh in einem noch heilbaren Stadium zu stellen.
Das Prostatakarzinom tritt überwiegend bei älteren Männern auf, die eine Symptomatik vielfach nicht mehr erleben würden. So hat sich seit zirka Anfang dieses Jahrtausends das »aktive Beobachten« (siehe unten) als brauchbares Konzept für Männer entwickelt, die sich (zumindest zunächst) keiner invasiven Therapie unterziehen möchten. Die Entscheidung zur Behandlung ist schwierig und vom Einzelfall abhängig. Therapeutische Optionen sind die Operation mit kompletter Entfernung der Prostata (Prostatektomie), die Strahlentherapie, die Hormontherapie und in manchen Fällen die Chemotherapie.
Prostatakrebs ist auch bei Tieren beschrieben; unter den Haustieren ist er beim Hund am häufigsten.
Die Prostata
Die Prostata oder Vorsteherdrüse ist eine akzessorische Geschlechtsdrüse aller männlichen Säugetiere einschließlich des Menschen. Sie liegt beim Menschen unterhalb der Harnblase und umkleidet die Harnröhre bis zum Beckenboden. Sie ähnelt in Größe und Form einer Kastanie. An ihrer Rückseite grenzt die Prostata an den Mastdarm (Rectum). Deswegen kann sie von dort aus mit dem Finger teilweise ertastet und eingeschränkt beurteilt werden. Aufgabe der Prostata ist die Abgabe eines Sekrets, das zusammen mit dem der Bläschendrüse, der Bulbourethraldrüse und den aus dem Hoden stammenden Samenzellen das Sperma bildet. Wachstum und Funktion der Vorsteherdrüse werden vorwiegend vom Geschlechtshormon Testosteron gesteuert.
Epidemiologie

Das Prostatakarzinom ist in Deutschland die häufigste diagnostizierte Krebserkrankung des Mannes und steht nach dem Bronchialkarzinom an zweiter Stelle bei den krebsbedingten Todesursachen der Männer. Rund 25 Prozent aller bei Männern jährlich neu auftretenden Krebserkrankungen betreffen die Prostata.[2] Das entspricht einer altersstandardisierten Inzidenzrate von etwa 99,1 auf 100.000 männliche Personen.[3] Nach einer aktuellen Statistik erkrankten in Deutschland 2018 jährlich ca. 65.000 Männer neu an Prostatakrebs.[3] Die beobachtbare, vermeintlich starke Zunahme in den letzten Jahrzehnten ist eher auf verbesserte diagnostische Methoden und eine allgemein höhere Lebenserwartung zurückzuführen als auf eine tatsächliche Zunahme der Fallzahlen.
| Jahr | 1980 | 1985 | 1990 | 1995 | 2000 | 2016 | 2018 |
|---|---|---|---|---|---|---|---|
| Jährliche Neuerkrankungen in Deutschland[3] |
16.800 | 21.600 | 27.500 | 35.400 | 44.800 | 58.780 | 65.200 |
Die jährliche Mortalität (Gesamtzahl der Todesfälle) liegt um 15.000.[3] Nach einer Übersichtsstudie von 2015 stieg die Rate von „schlafendem“ (latentem) Prostatakrebs bei der Autopsie von Personen, die durch andere Ursachen gestorben waren, von 5 % in der Altersgruppe bis 30 Jahre auf 59 % in der Altersgruppe ab 80 Jahre.[4] Eine ähnliche Übersichtsstudie, ebenfalls von 2015, zeigte auf einer etwas abweichenden Datengrundlage denselben Trend.[5]
Es gibt starke geographische und ethnische Unterschiede in der Häufigkeit: Männer schwarzafrikanischen Ursprungs haben die höchste Inzidenzrate, am niedrigsten ist sie bei Asiaten.[6] Auszüge aus nationalen Krebsregistern aus der Zeit bis 1980 erbrachten, dass die altersstandardisierte Erkrankungsrate mit etwa 100/100.000 Personen in Deutschland und Österreich in den letzten 20 Jahren relativ stabil war, sie aber in vielen europäischen Ländern auf das 2-3 fache angestiegen war, namentlich in Litauen um das achtfache[7]. Im gleichen Zeitraum nahm die Mortalität in den meisten europäischen Ländern (außer in einigen osteuropäischen Ländern) langsam ab und lag im Mittel zwischen 23 und 35 pro 100.000 Personen. Die Autoren der Analyse führen diesen Anstieg der Inzidenz auf eine Überdiagnostik durch ein anlassloses PSA-Screening zurück[7].
Die Daten für die weltweiten Erkrankungsraten sind nicht zuverlässig, da sie zum Teil auf Schätzungen beruhen und die diagnostischen Möglichkeiten in den einzelnen Regionen sehr differieren. Die auf Daten der Internationalen Agentur für Krebsforschung (IARC) beruhende Erhebung GLOBOCAN gibt für das Jahr 2002 insgesamt knapp 680.000 Neuerkrankungen und etwa 220.000 Todesfälle an. Hiernach ist die jährliche Inzidenzrate in Zentralasien mit weniger als 3/100.000 Einwohnern am niedrigsten, die höchste ist auf dem nordamerikanischen Kontinent mit über 160/100.000 Einwohnern zu verzeichnen.[8]
Risikofaktoren und protektive Faktoren
Alter
Der wichtigste Risikofaktor ist das Alter. Das zeigen epidemiologische Untersuchungen des Zentrums für Krebsregisterdaten. In der Altersgruppe 45–49 Jahre kommt es in Deutschland bei 100.000 Männern zu 17,3 Neuerkrankungen pro Jahr. In der Altersgruppe 70–74 Jahre sind es 653,7.[9.1]
Genetik
Die Ursache der Erkrankung ist bisher weitgehend unbekannt. Die genetische Disposition spielt bei der Entstehung der Erkrankung eine Rolle (familiäre Häufung). Daher gelten Männer, deren Väter oder Brüder Prostatakrebs hatten, als Risikopatienten mit etwa doppeltem Erkrankungsrisiko.[10] Das gilt insbesondere, wenn die Vorerkrankten bereits in jungen Jahren betroffen waren.[9.1] Nun konnte auch in einer Studie gezeigt werden, dass dem beim jungen Mann auftretenden Adenokarzinom der Prostata eine andere Pathophysiologie zugrunde liegt. Es zeigte sich, dass der testosteronbindende Androgenrezeptor eine erhöhte Aktivität aufweist, wodurch eine ganze Reihe von Genen verändert und die Entstehung eines Karzinoms erleichtert wird.[11] Männer mit familiärem Risiko sollen ab 45 Jahren, Männer mit pathologischen Genvarianten sollen ab dem Alter von 40 Jahren auf eine Frühuntersuchung angesprochen werden.[9.2]
Lebensweise
Die Leitlinienautoren sahen 2025 keine eindeutigen Belege für eine Beeinflussung des Risikos speziell für Prostatakrebs durch die Ernährung. Vielmehr wird eine allgemein gesunde Lebensführung empfohlen. Man unterstützt die Punkte, die auch in der US-amerikanischen Leitlinie aufgeführt werden:[9.1]
- normales Körpergewicht (Vermeiden einer Adipositas)
- körperliche Aktivität (mindestens 30 Minuten am Tag, 5 Mal pro Woche)
- gesunde Ernährung mit Schwerpunkt auf pflanzlicher Kost, wenig rotes Fleisch
- wenig Alkohol (maximal 2 Drinks pro Tag)
Diese Empfehlung erfolgt in dem Bewusstsein, dass eine Lebensführung, die das Risiko für das Prostatakarzinom senken soll, auch das gesundheitliche Gesamtrisiko senken soll. Für weitere Ernährungsempfehlungen reicht die Datenlage nicht aus.[9.1]
Es konnten keine Hinweise darauf gefunden werden, dass die Sterilisation (Vasektomie) das Erkrankungsrisiko erhöht.[12]
Nach einer 2003 veröffentlichten Studie soll häufiges Ejakulieren in jüngeren Jahren das Erkrankungsrisiko senken.[13] Australische Wissenschaftler verglichen Daten zu Sexualpraktiken von 1079 Prostatakrebs-Patienten mit denen von 1259 gesunden Männern im Alter zwischen 20 und 50 Jahren. Ihr Ergebnis: Zwanzigjährige, die öfter als viermal pro Woche ejakulieren, senken ihr Risiko für Prostatakrebs um ein Drittel. Methodisch ist hierbei das Ursache-Wirkungs-Verhältnis nicht geklärt; es könnte sein, dass Männer mit einem gesunden, leistungsfähigen Genitaltrakt öfter ejakulieren und die Gesundheit der Genitalien die eigentliche Ursache ist, weshalb sie später auch nicht so häufig erkranken. Im Gegensatz dazu hatten frühere Studien häufige Sexualkontakte mit einem deutlich erhöhten Risiko für Prostatakrebs in Zusammenhang gebracht. Dies könnte jedoch, nach Ansicht der australischen Forscher, durch die höhere Infektionsgefahr bedingt sein. Betrachtet man die Zahl der Ejakulationen insgesamt, so hätten diese einen schützenden Effekt, weil durch die häufige Bildung von Samenflüssigkeit krebserregende Substanzen aus der Prostata herausgeschwemmt werden. Auch würden die Prostatazellen auf diese Art zum Ausreifen angeregt, was sie für Karzinogene weniger anfällig machen könnte. Eine 2016 veröffentlichte Studie (Datenbasis über 30.000 Männer) zieht ebenfalls den Schluss, dass das Erkrankungsrisiko mit steigender Ejakulationsfrequenz sinkt.[14] Die Autoren räumen aber auch ein, dass sexuell aktive Männer möglicherweise seltener zu Vorsorgeuntersuchungen gehen, so dass potentielle Erkrankungen in dieser Untersuchungsgruppe häufiger unentdeckt bleiben. Für ein gesenktes Erkrankungsrisiko werden verschiedene physiologische Gründe vorgeschlagen. So kann häufiges Ejakulieren die Funktion und Teilungsgeschwindigkeit der randständigen Epithelzellen beeinflussen, so dass eine frühe Tumorgenese behindert wird.
Testosteronbehandlung
Man kann davon ausgehen, dass eine Behandlung mit Testosteron ein vorbestehendes Prostatakarzinom im Wachstum beschleunigt. Deshalb soll vor einer Testosteronbehandlung ein Prostatakarzinom mittels PSA-Wertbestimmung und digital-rektaler Untersuchung ausgeschlossen werden.[9.1]
Molekularbiologische Aspekte des Prostatakarzinoms
Wie allen Neoplasien liegt auch dem Prostatakarzinom letztlich die irreversible Veränderung des Erbgutes einer einzigen Zelle zugrunde. Alle Krebszellen sind Abkömmlinge (Klone) dieser Zelle. Verkomplizierend kommt hinzu, dass sich deren Erbgut weiter verändert, da die physiologischen Vorgänge, die DNA-Schäden reparieren oder mutierte normale Körperzellen absterben lassen würden (Apoptose), in Krebszellen nicht zum Tragen kommen. Mit der Zeit entwickelt sich daher ein Mosaik aus Zellen mit unterschiedlich stark verändertem Genom. Klinisch entspricht dem ein inhomogenes Erscheinungsbild des Tumors und ein zunehmendes „Bösartigerwerden“ über die Jahre.
Anders als viele andere epitheliale Malignome hat das Prostatakarzinom keine typische Adenom-Karzinom-Sequenz und auch kein spezifisches Mutationsmuster. Stattdessen kommen sehr heterogene genomische Veränderungen in Form von Punktmutationen an verschiedenen Stellen, Verlusten von Allelen oder ganzen Chromosomen und bisweilen zusätzlich Polyploidie vor. Häufig sind jedoch in einem späteren (metastasierten) Stadium zumindest auch klassische Tumorsuppressorgene wie TP53 von Deletionen oder Mutationen betroffen. Eine wichtige Rolle scheinen Veränderungen des den Androgenrezeptor codierenden Gens zu spielen. Derzeit sind mindestens 17 genetisch verschiedene Zelllinien des Prostatakarzinoms bekannt.[15]
Für Träger einer BRCA1- oder BRCA2-Mutation besteht ein erhöhtes Risiko für das Entstehen von Prostatakrebs.[16]
Symptomatik
In frühen Stadien ist Prostatakrebs nahezu immer symptomlos. Hauptbeschwerden ergeben sich beim fortgeschrittenen Karzinom aus der Blockade des Harnabflusses und bestehen somit in Störungen der Miktion (Urinieren). Möglich sind ein verzögerter Beginn, eine verlängerte Miktion mit schwachem Strahl, Nachtropfen oder die Unterbrechung des Harnstrahls während des Wasserlassens. Oft bleibt Restharn in der Blase zurück. Irritative Beschwerden sind vermehrter oder überwiegend nächtlich auftretender Harndrang (Nykturie), häufiges Lassen geringer Urinmengen (Pollakisurie), erschwertes Wasserlassen (Dysurie) oder Schmerzen beim Wasserlassen (Algurie). Durch Druckschädigung von Nerven des Kreuzbeinbereichs kann es zu Erektionsstörungen kommen. Sichtbares Blut im Urin (Hämaturie) oder Ejakulat (Hämatospermie) ist hingegen selten.
Beschwerden können im fortgeschrittenen Stadium mit Metastasierung auch primär durch die Metastasen entstehen, während das Prostatakarzinom klinisch stumm bleibt (okkultes Karzinom). Am häufigsten sind hier Schmerzen der Wirbelsäule und des Beckens. Bei starker metastatischer Durchsetzung kann es zu spontanen Knochenbrüchen ohne Trauma, sogenannten pathologischen Frakturen, kommen. Da häufig die Wirbelsäule die erste Aussaatstrecke bildet, sind komplexe neurologische Ausfälle durch Rückenmarksverletzung wie Querschnittsyndrome oder das Cauda-equina-Syndrom nicht selten. Lymphknotenmetastasen können zu Lymphödemen der Beine oder des Hodensacks führen. Insgesamt stellen jedoch Knochenmetastasen für die meisten Patienten die vorherrschende Manifestation der Erkrankung dar und sind auch die hauptsächliche Ursache für die Morbidität und Mortalität des Prostatakarzinoms.[17]
Fortgeschritten metastasierte Tumoren führen in der Regel auch zu Allgemeinsymptomen wie Anämie und ungewolltem Gewichtsverlust.
Früherkennung
Maßnahmen zur Früherkennung können Prostatakrebs nicht verhindern. Sie dienen vielmehr dazu, Tumore in einem frühen Stadium zu erkennen und die Sterblichkeit zu vermindern. Dabei ist zu beachten, dass sich durch die Feststellung der Diagnose in einem früheren Stadium automatisch die Überlebenszeit verlängert, auch wenn der Todeszeitpunkt der gleiche ist. Früherkennung kann bei 3 von 1000 Männern den Tod durch Prostatakrebs verhindern. Ob dadurch auch die Gesamtsterblichkeit dieser 1000 Männer geringer ist, kann nicht nachgewiesen werden.[9.2]
Männer ab einem Alter von 45 Jahren mit einer Lebenserwartung von mehr als 10 Jahren, die eine Früherkennungsuntersuchung wünschen, sollen ergebnisoffen über Vor- und Nachteile beraten werden. Denjenigen, die nach dieser Beratung eine Untersuchung wünschen, soll eine Bestimmung des PSA-Wertes angeboten werden.
Das Abtasten der Prostata über den Enddarm und der transrektale Ultraschall werden in der Früherkennung nicht mehr als geeignete Maßnahme angesehen. Ist der PSA-Wert auffällig, soll zur weiteren Diagnostik eine Magnetresonanztomografie (MRT) durchgeführt werden.[9.2] Der Gemeinsame Bundesausschuss prüft – Stand Oktober 2025 – die Möglichkeit, über die Krankenkassen ein Früherkennungsprogramm mit beiden Maßnahmen anzubieten. Ein Ergebnis ist im Oktober 2027 zu erwarten.[18]
Die im Oktober 2025 veröffentlichte European Study of Prostate Cancer Screening (finanziert durch die Dutch Cancer Society) beobachtete Nutzen und Risiko des PSA-Screenings über einen Zeitraum von 23 Jahren. Die Autoren bewerteten das PSA-Screening grundsätzlich positiv: Das Risiko, an Prostatakrebs zu versterben, war in der Screening-Gruppe um 13 % niedriger als in der Kontrollgruppe. Die negativen Auswirkungen des PSA-Screenings hätten sich über den Beobachtungszeitraum verringert. Für die Zukunft solle ein risikoorientierter Zugang die Überdiagnostik vermindern, ohne die Vorteile des PSA-Screenings zu verlieren.[19] Für die Kalkulation des Risikos können die Faktoren Alter, familiäre Belastung und genetische Prädisposition herangezogen werden.[9.2] Patienten haben die Möglichkeit, ihr Risiko selbst einzustufen. Dazu steht ein Prostata-Risikokalkulator im Internet zur Verfügung.[20]
In der Zwischenzeit bieten noch viele Arztpraxen die Früherkennung als individuelle Gesundheitsleistung (IGeL) an.
Stellungnahmen von Institutionen im Gesundheitswesen zur Früherkennung des Prostatakarzinoms
Der IGeL-Monitor des MD Bund (Medizinischer Dienst Bund) geht 2012 (2017 aktualisiert) davon aus, dass pro Mann, der durch die Früherkennung vor dem Tode bewahrt würde, 30 Männer die Diagnose Prostatakarzinom und die Folgen dieser Diagnose in Kauf nehmen müssen. Wichtig sei jedoch, dass jeder Mann den Nutzen und den Schaden selbst bewertet.[21]
Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) nahm im Juni 2025 zu dem, in der aktuellen S3-Leitlinie Prostatakarzinom betrachteten Thema Früherkennung, wie folgt Stellung:
„Angesichts der problematischen PSA-Testung gilt es nicht, möglichst breit zu testen und möglichst viel zu finden. Um das Nutzen-Schaden-Verhältnis zu optimieren, sollte die Diagnostik (wie in Skandinavien) gemäß individueller informierter Entscheidung mit dem Blick auf Alter, Intervalle und Grenzwerte so fokussiert werden, dass klinisch signifikanter Prostatakrebs gefunden werden kann.“
Die Deutsche Krebshilfe fasst im Oktober 2023 zusammen:
„Die rektale Untersuchung ist zur Frühdiagnose nicht geeignet.“
Die Bestimmung des PSA-Wertes bietet Vor- und Nachteile. Im mittleren Lebensalter (45–54 Jahre) habe der PSA-Wert eine hohe Vorhersagekraft, im weiteren Verlauf des Lebens einen Prostatakrebs (PK) zu entwickeln. Um die Aussagekraft des PSA-Werts im späteren Lebensalter zu erläutern, dient eine Gegenüberstellung von Männern mit PSA-Test und ohne:
| Diagnose PK | Diagnose Metastasen | Tod durch PK | |
|---|---|---|---|
| ohne PSA | 97 | 25 | 15 |
| mit PSA | 155 | 17 | 11 |
Durch eine regelmäßige Bestimmung des PSA-Wertes ergibt sich also häufiger eine Krebsdiagnose, auch bei Männern, die nie Beschwerden durch einen PK bekommen und irgendwann an etwas anderem versterben. Weil mehr PK entdeckt werden, werden auch mehr operiert, es gibt weniger PK-Metastasen und es sterben weniger Männer an PK. Die Deutsche Krebshilfe weist – wie auch die anderen Institutionen – darauf hin, dass jeder Patient die Vor- und Nachteile der Früherkennung nach entsprechender Information selbst bewerten muss. Die daraus resultierende Entscheidung ist von den behandelnden Ärzten zu respektieren.[23]
Diagnostik



Die Diagnostik bei Männern ohne Krankheitsverdacht entspricht einer Früherkennungsuntersuchung und beginnt mit der Bestimmung des PSA-Wertes im Blut.[9.2]
Die Tastuntersuchung der Prostata vom Enddarm aus (digital-rektale Untersuchung) ist wenig aussagekräftig und wird nicht mehr empfohlen.[9.2]
Bildgebende Verfahren
Bei Männern mit einem PSA-Wert über 3 ng/ml, mit erhöhtem Risikoprofil, oder mit klinischem Verdacht auf einen Prostatakrebs wird eine Magnetresonanztomografie durchgeführt. Findet sich hierbei ein Herdbefund, kann die Dignität durch weitere Blut- und Urinuntersuchungen genauer ermittelt werden. Sogenannte Biomarker wie PCA3 erlauben eine genauere Unterscheidung zwischen gutartigen und bösartigen Befunden.[9.4] Erhärtet sich dabei der Krankheitsverdacht, erfolgt die Stanzbiopsie der Prostata entweder vom Enddarm oder vom Damm aus, um Material für eine feingewebliche Untersuchung zu gewinnen.[9.3] Wird ein Prostatakarzinom in einem frühen Stadium festgestellt, sind keine weiteren bildgebenden Verfahren erforderlich. Eine Metastasierung ist dann sehr unwahrscheinlich.[9.5] Ist der Tumor schon weiter fortgeschritten, muss von einer Metastasierung in den Körper ausgegangen werden. Um dies zu beurteilen, ist die Positronen-Emissions-Tomographie (PET) die am besten geeignete Untersuchungsmethode.[9.5]
Stanzbiopsie
Nach dem MRT kann schon die Diagnose eines Tumors in der Prostata gestellt und die Stadienbestimmung (s. u.) vorgenommen werden. Beweisend für ein Karzinom ist aber letztlich erst der Nachweis von Krebszellen in einer bioptisch entnommenen Gewebeprobe. Die Biopsie wird perineal oder transrektal durchgeführt. Um den fraglichen Herd zu treffen, ist eine gleichzeitige Bildgebung notwendig. Dabei kann eine KI-gestützte Ultraschallortung hilfreich sein. Andere Untersuchungsmethoden unter Verwendung von Ultraschall haben keinen Stellenwert mehr.[9.6] Es werden mit einer Hohlnadel insgesamt 10–12 Gewebeproben entnommen. Zur Verminderung des Infektionsrisikos wird prophylaktisch ein Antibiotikum verabreicht. Die Biopsie erfolgt in lokaler Infiltrationsanaesthesie.[9.7]
Ein Pathologe begutachtet das Prostatagewebe und stellt seine Diagnose (s. u.).
Diagnostik zur Stadienbestimmung bei nachgewiesener Erkrankung
Nachdem die Diagnose Prostatakrebs gesichert ist, wird dessen Ausdehnung untersucht. Dabei sind die Größe des Tumors, eventuell befallende regionale Lymphknoten und Metastasen von Interesse. Je nach Befund erfolgt dann die Stadieneinteilung nach dem System der internationalen Vereinigung gegen den Krebs (UICC) mittels der TNM-Klassifikation.[9.8] Die Bestimmung der Tumorgröße (T-Kategorie) erfolgt mittels digitaler-rektaler Untersuchung und Magnetresonanztomografie (MRT). Ist der Tumor klein, ist eine Metastasierung sehr unwahrscheinlich und eine weitere Bildgebung nicht erforderlich.[9.8] Bei großen Tumoren wird für die Suche nach Metastasen die Positronen-Emissions-Tomografie (PET) eingesetzt.[9.8]
Tumorstadien
Staging (TNM-System)
Bei der Beurteilung des Tumorstadiums nach dem TNM-System werden Größe und örtliche Ausdehnung des Prostatatumors (T), Lymphknotenbefall (N, von engl. node ‚Knoten‘) und Metastasen (M) berücksichtigt. Die Ziffern hinter den Buchstaben stehen für Größe und Ausdehnung des Primärtumors (T1–T4), das Vorliegen von befallenen Lymphknoten (N0–N1) sowie das Vorhandensein und die Verteilung von Fernmetastasen (M0-M1c).
Ein recht guter Prädiktor für die Entdifferenzierung, die lokale Invasion der Nachbarorgane und die Wahrscheinlichkeit der Fernmetastasierung ist auch die Tumorgröße. Die „Schwelle der Kurabilität“, also die Größe des Tumors, bis zu welcher man eine Behandlung mit der Zielsetzung der Heilung (kurative Behandlung) als möglich erachtet, wird bei 4 cm³ angesetzt. Ist diese Schwelle überschritten, so ist eine Heilung in der Regel nicht mehr möglich. Jedoch können durchaus auch kleinere Tumoren bereits metastasiert sein und sich somit einer kurativen Behandlung entziehen.[24]
| Stadium | Beschreibung |
|---|---|
| Tx | Es kann keine Aussage zur Ausdehnung des Primärtumors getroffen werden. |
| T1 | Der Tumor ist klein und nicht tastbar. Er wird zufällig im Rahmen einer Prostataoperation wegen Prostatavergrößerung oder erhöhter PSA-Werte gefunden (Inzidentaltumor). |
| T1a | Der Tumor befällt höchstens 5 % des Gewebes. |
| T1b | Der Tumor befällt mehr als 5 % des Gewebes. |
| T1c | Der Tumor wurde durch eine Nadelbiopsie diagnostiziert. |
| T2 | Der Tumor liegt noch innerhalb der Prostatakapsel. |
| T2a | Der Tumor befällt höchstens 50 % eines Seitenlappens. |
| T2b | Der Tumor befällt mehr als 50 % eines Seitenlappens. |
| T2c | Der Tumor befällt beide Seitenlappen. |
| T3 | Der Tumor hat sich über die Prostatakapsel hinaus ausgebreitet; eine Ausdehnung in die Prostataspitze oder in die Prostatakapsel (aber nicht darüber hinaus) wird nicht als T3-, sondern als T2-Tumor gewertet. |
| T3a | Der Tumor hat sich über die Prostatakapsel ausgebreitet, ohne die Samenblasen zu befallen. |
| T3b | Der Tumor hat sich über die Prostatakapsel ausgebreitet und befällt die Samenblasen. |
| T4 | Der Tumor hat Nachbarstrukturen befallen (infiltriert) oder ist fixiert (unverschieblich). |
| Nx | Es kann keine Aussage zu regionären Lymphknotenmetastasen getroffen werden. |
| N0 | Keine Metastasen in den regionären Lymphknoten. |
| N1 | Metastasen in den regionären Lymphknoten. |
| M0 | Keine Fernmetastasen nachweisbar. |
| M1 | Der Tumor hat Fernmetastasen gebildet. |
| M1a | Metastasen in anderen Lymphknoten (nichtregionale Lymphknoten). |
| M1b | Metastasen in den Knochen. |
| M1c | Metastasen in anderen Organen und/oder Strukturen. |
An der Einordnung in das TNM-Schema orientiert sich die Behandlung. Auch die Prognose kann unter Hinzuziehung weiterer Parameter abgeschätzt werden.
Ein anderes Schema der Stadieneinteilung ist das nach Whitmore-Jewett (modifiziert nach Hopkins). Hier werden die Grade A (mikroskopisches Karzinom, praktisch immer inzidentiell – entspricht T1), B (makroskopisch, auf die Prostata begrenzt – entspricht T2); C (organüberschreitend, auf das kleine Becken begrenzt – entspricht T3/4M0) und D (mit Fernmetastasen – entspricht T1–4M1) unterschieden. Dieses Schema wird im angloamerikanischen Raum bevorzugt, ist aber in Deutschland nicht üblich.
Pathologie und Histopathologie
Stanzbiopsien und Operationspräparate werden von einem Pathologen untersucht.
Makroskopische Pathologie

Makroskopisch (mit bloßem Auge) erscheint das Karzinom meist gelb oder weißlich, relativ homogen und unscharf begrenzt. Mehrheitlich geht es von den Epithelien der peripheren Drüsenanteile aus, zu etwa 85 % in den hinteren (rektalen) Anteilen der Vorsteherdrüse und breitet sich in den äußeren Zonen des Organs aus. Zur Verlegung der Harnröhre mit Beschwerden des Harnlassens kommt es daher erst spät, meist nachdem die Organkapsel schon durchbrochen wurde.
Ausgedehnte Karzinome der Stadien T3/T4 können die Samenblasen, die Harnblase, den Beckenboden oder das Rektum infiltrieren. Die Metastasierung ist zunächst lymphogen (über die Lymphbahnen) in die ortständigen Lymphknoten. Häufig erfolgt später eine hämatogene Aussaat (über die Blutbahn). Typisch sind Knochenmetastasen in Becken, Kreuzbein und Lendenwirbelsäule, Oberschenkelknochen, Brustwirbelsäule und Rippen. So ist bei 80 % bis 90 % der Patienten mit einem metastasierenden Prostatakarzinom das Achsenskelett (Wirbelsäule, Becken und Strukturen, die am Rumpf oder nahe am Rumpf gelegen sind) betroffen.[17] Diese sind fast immer osteoblastisch (knochenbildend). Fernmetastasen in Lunge und Leber durch hämatogene Aussaat (über den Blutkreislauf) sind seltener.[26]
Mikroskopische Pathologie
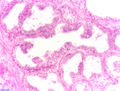
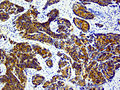
97 % aller Prostatatumoren sind Adenokarzinome, das heißt, sie entstehen aus entarteten Drüsenzellen. Ein Übergangsstadium zum manifesten Krebs wird als prostatische intraepitheliale Neoplasie (PIN) bezeichnet und entspricht einem Carcinoma in situ. Beim eigentlichen Karzinom kommen verschiedene histopathologische Wachstumsmuster vor, auch gleichzeitig nebeneinander: glandulär beziehungsweise azinär (drüsenartig), kribriform (siebartig) und solide. Das Ausmaß der Entdifferenzierung ist Grundlage des Gradings. 40–50 % der Tumoren liegen bei Diagnosestellung multifokal vor.[24]
- Normales Prostatagewebe
- Prostatische intraepitheliale Neoplasie (PIN)
- Karzinom vom azinären Typ
- Entdifferenziertes Karzinom
- Knochen- und Weichteilmetastase eines Prostatakarzinoms mit immunhistochemischem Nachweis einer PSA-Expression (braun)
Die Nicht-Adenokarzinome (weniger als drei Prozent) sind meist urothelialer Herkunft, leiten sich also aus dem Übergangsgewebe der Harnröhre oder -blase ab (siehe Blasenkrebs). Äußerst selten sind Sarkome (Leiomyosarkom, Fibrosarkom, Rhabdomyosarkom) des Stromas beim Erwachsenen. Bei Kindern sind Rhabdomyosarkome die häufigste Form des Prostatakrebses, werden aber nicht wie bei erwachsenen Patienten als Prostatakarzinom aufgefasst, sondern als Weichteilsarkom.[27][28]
Tumorgrad und Gleason-Score
Bei der mikroskopischen Untersuchung des entnommenen Gewebes werden die biologischen Eigenschaften des Tumors genauer bestimmt und seine Bösartigkeit ermittelt. So beschreibt ein besonderes Einordnungsschema (G: Histopathologisches Grading), wie stark sich die Tumorzellen mikroskopisch von normalen, „ausgereiften“ Zellen unterscheiden.
Zum Grading des Prostatakarzinoms wird entsprechend der S3-Leitlinien zur Früherkennung, Diagnose und Therapie des Prostatakarzinoms der Gleason-Score verwendet.[29] Dabei wird nach dem histologischen Bild in der Stanzbiopsie das am schlechtesten differenzierte und das am häufigsten vorkommende Tumorgewebe mit Punktwerten zwischen 1 und 5 (zusammen also zwischen 2 und 10) bewertet und addiert. Bei einer bereits erfolgten Operation wird der häufigste und der am zweithäufigsten vorkommende Gleason-Grad in der gesamten Prostata addiert. Die beiden addierten Gleason-Grade müssen in der richtigen Reihenfolge und in der Stanzbiopsie in Prozent (des Gesamttumors und des gesamten gewonnenen Gewebes) angegeben werden. Ein Gleason-Score 3+4 stellt einen besser differenzierten Grad dar, als Gleason-Score 4+3, obwohl die Summe gleich ist. Ihre Summe wird in der Stanzbiopsie demnach anders interpretiert als im Operationspräparat. Eine Besonderheit ist, dass die Gleason-Grade 1 und 2 in der Stanzbiopsie nicht diagnostiziert werden können.[30]
Der Gleason-Score ist neben der Tumorgröße, dem Vorliegen von Lymphknoten- und Fernmetastasen (TNM-Klassifikation) ein wichtiger Prognosefaktor. Ein Gleason-Score kann nur bei Vorliegen eines nicht vorbehandelten Adenokarzinoms der Prostata erstellt werden, für Urothelkarzinome und neuroendokrine Tumoren wird ein anderes Grading-System benutzt.[29]
ISUP-Gruppen
Die Internationale Gesellschaft für Urologische Pathologie (ISUP) teilt Prostatakarzinome nach ihrer mutmaßlichen Aggressivität und Wachstumsgeschwindigkeit in Zusammenschau mit dem Gleason-Score in fünf Gruppen ein:[31][32]
ISUP-Gruppe 1: Gleason-Score 6, der Tumor wächst langsam und ist auf die Prostata beschränkt
ISUP-Gruppe 2: Gleason-Score 3+4, der Tumor wächst langsam, Metastasen sind unwahrscheinlich
ISUP-Gruppe 3: Gleason-Score 4+3, der Tumor wächst mäßig und ist nicht mehr auf die Prostata beschränkt
ISUP-Gruppe 4: Gleason-Score 8, der Tumor wächst schnell, Fernmetastasen wahrscheinlich
ISUP-Gruppe 5: Gleason-Score 9+10, der Tumor wächst sehr schnell, Fernmetastasen sehr wahrscheinlich
Beurteilung der Prognose
Wichtigste Faktoren für die Einschätzung der Prognose sind das Tumorstadium nach TNM-Klassifikation, der PSA-Blutwert, die Differenzierung des Tumors nach dem Gleason-Score, beziehungsweise die ISUP-Gruppe und im Fall einer Operation die Beurteilung der Resektionsränder im Hinblick auf die Freiheit von Tumorzellen (Frage der vollständigen Resektion).[9.9]
Patienten mit metastasiertem, kastrationsresistentem Prostatakarzinom profitieren eventuell von einer humangenetischen Untersuchung auf das Vorhandensein von BRCA-Mutationen (Brustkrebsgen-Mutationen). In diesem Fall käme eine Therapie mit PARP-Inhibitoren in Frage.[9.9]
Therapie
Die Empfehlung zu bestimmten Therapieoptionen richtet sich nach dem Tumorstadium (TNM-System) und dem Risikoprofil (ISUP-Gruppe, Alter, Begleiterkrankungen). Strategien mit der Absicht einer Heilung (kurativ) und solche ohne diese Absicht (palliativ) stehen je nach Situation zur Verfügung. Bei der Eröffnung der Therapieoptionen und insbesondere während einer palliativen Therapie bedarf der Patient einer besonders intensiven Beratung und Betreuung. Die Entscheidung des Patienten für oder gegen eine Option ist stets zu respektieren.[9.10]
Aktive Überwachung
Die aktive Überwachung (engl. active surveillance) ist eine Strategie für die Patienten mit einem lokalisierten (auf die Prostata beschränkten), heilbaren Prostatakrebs (PK). Wie der Begriff schon andeutet, werden hier zunächst keine invasiven therapeutischen Maßnahmen ergriffen. Erst bei Überschreiten zuvor definierter Grenzen werden weitergehende Therapiemaßnahmen ergriffen. Die Überwachung besteht bei Tumoren der ISUP-Gruppe 1 aus einer PSA-Kontrolle alle 6 Monate über 2 Jahre, bei Tumoren der ISUP-Gruppe 2 aus einer PSA-Kontrolle alle 3 Monate über 2 Jahre. Dazu kommen MRT-Untersuchungen und erneute Biopsien in größeren zeitlichen Abständen. Mit der aktiven Überwachung hat der Patient eine Therapieoption, die eine höhere Lebensqualität gewährleistet, als es bei einer Operation der Fall wäre. Deren Nebenwirkungen wie Inkontinenz oder sexuelle Funktionsstörungen werden vermieden. Definitionsgemäß hat Active Surveillance bei ansonsten gesunden und für eine kurative Therapie geeigneten Patienten das Ziel, unter genauer Überwachung einschließlich regelmäßiger Kontrollbiopsien die rechtzeitige kurative Behandlung bis zu einem Zeitpunkt aufzuschieben, an dem sich möglicherweise die Tumorbiologie oder der Wunsch des Patienten ändern. Als sekundäre Behandlung wird dann in den meisten Fällen die radikale Prostatektomie gewählt (48 %). Auch nach 10 oder 15 Jahren der aktiven Überwachung ist die PK-spezifische Sterblichkeit gegenüber den operierten Patienten nicht wesentlich erhöht. Aktive Überwachung ist die Standardempfehlung für Patienten mit einem PK mit niedrigem Risiko.[9.10] Die Strategie des watchful waiting (Beobachten und Abwarten), verfolgt nicht das Ziel der Heilung. Sie kommt zur Anwendung bei Patienten mit kurzer Lebenserwartung und/oder schweren Begleiterkrankungen, die die Lebenserwartung begrenzen. Beim watchful waiting steht das Bemühen im Vordergrund, den Patienten nicht unnötig mit diagnostischen oder therapeutischen Maßnahmen zu belasten. Erst wenn der PK Symptome verursacht und der Patient deren Behandlung wünscht, werden palliative Maßnahmen ergriffen.[9.10]
Operation
Bei lokal begrenztem Prostatakarzinom (T1/2) und guter Konstitution ist die radikale (vollständige) Operation der Prostata, bei der Prostata, Samenbläschen und die regionalen Lymphknoten entfernt werden, eine traditionelle Methode. Diese so genannte „radikale Prostatektomie“ (RPE) kann auf vier unterschiedliche Arten durchgeführt werden:
- als retropubische radikale Prostatektomie (RRP)
- als radikale perineale Prostatektomie (RPP) durch Schnitt am Damm (zwischen After und Hodensack)
- minimalinvasiv – laparoskopisch
- roboterassistiert (RARP)
RRP wird vom Bauch aus durchgeführt, RPP wird extraperitoneal, also ohne Eröffnung der Bauchhöhle, ausgeführt. Die RPP ist weniger zeitaufwändig und mit geringeren Blutungen verbunden als die RRP, aber der Zugang ist relativ schmal. Ein Nachteil ist die fehlende Entfernung der Beckenlymphknoten bei der RPP, so dass ein zweiter Eingriff mittels laparoskopischer pelviner (auf das Becken bezogener) Lymphadenektomie manchmal notwendig ist. Einzelne Zentren haben Techniken publiziert, welche die Lymphknotenentfernung ermöglichen.[33]
Bei der minimalinvasiven Methode wird mittels Bauchspiegelungstechnik über einige kleine Schnitte die Prostata operiert. Vorteil im Vergleich zur „offenen“ Operation ist hier vor allem der zumeist geringere Blutverlust und die kleinen Wunden.
Eine Weiterentwicklung der „minimalinvasiven“ Technik ist die roboterassistierte Prostatektomie. Hier wird mit Hilfe eines Operationsroboters die laparoskopische Technik durchgeführt. Der Roboter wird dabei vom Operateur mittels einer speziellen Konsole fernbedient und führt keine eigenständigen Bewegungen aus. Vorteil für den Operateur gegenüber der Standard-Laparoskopie ist hierbei die nahezu uneingeschränkte Beweglichkeit der Instrumente, die hervorragende Sicht (dreidimensional über ein Doppel-Optik-System) und die Feinheit der Bewegung, da der Roboter etwa das natürliche Zittern der Hand ausgleicht. Nachteil der Robotertechnik gegenüber der „Standard-Laparoskopie“ sind die vergleichsweise hohen Anschaffungs- und Unterhaltskosten für das Krankenhaus, so dass in Deutschland bisher nur wenige Zentren auf diese Technik zurückgreifen können, bei einigen Abteilungen wird eine private Zuzahlung zur Deckung der Materialkosten verlangt, da die Krankenkassen diese derzeit nicht übernehmen. Eine Verbesserung der Operationsergebnisse durch die Robotertechnik konnte bisher wissenschaftlich nicht belegt werden.
Gelingt es bei der Operation, den Tumor vollständig zu entfernen, ist eine Heilung möglich, und die Prognose für ein Langzeitüberleben (fünf Jahre oder mehr) liegt zwischen 80 und 90 Prozent. Gemäß der weltweit größten urologischen Studie (52.000 Patienten) zur Behandlung des lokalisierten Prostatakrebses ist die Operation bei Patienten mit geringem oder mittlerem Risiko der Bestrahlung nach fünf Jahren im Ergebnis geringgradig unterlegen. Den größten Vorteil zeigte die Bestrahlung im Vergleich zur Operation insbesondere bei Patienten, die ein hohes Risiko haben, Metastasen zu entwickeln.[34]
Das Risiko, an der Operation oder ihren Folgen zu versterben, beträgt etwa 1,5 Prozent.[35] Ein relevantes Risiko der Operation ist in erster Linie die Gefahr der langfristigen Harninkontinenz und beträgt je nach Studie zwischen 2 und 40 Prozent.[36] So benötigten etwa in einer britischen Studie aus dem Jahr 2006 27,8 % der Patienten täglich bis zu eine Einlage.[37]
Zum Verlust der Erektionsfähigkeit (erektile Dysfunktion) in Folge einer Verletzung der Nervi cavernosi (Äste der parasympathischen Beckeninnervation) kommt es in etwa 80 % der Fälle.[38] Ein trockener Orgasmus ist meist weiterhin möglich[39], eine Studie zeigt, dass 71 % der operierten Männer orgasmusfähig waren.[40] Verletzungen des Nervus obturatorius, die im Rahmen der Lymphknotenentfernung auftreten können, oder des Rektums sind selten. In fünf bis 20 Prozent der Fälle kommt es, bedingt durch die Lymphknotenentfernung, zu einer Lymphozele. Als Spätfolge tritt in etwa 32 % der Fälle eine Verengung der Verbindungsstelle zwischen Harnröhre und Blase (Anastomose) auf, die so genannte Anastomosenstriktur.[35]
Etliche Zentren bieten eine „nerverhaltende“ Operationsmethode (nach Patrick Craig Walsh) an, bei der die kavernösen Nerven, die in unmittelbarer Lagebeziehung zur Prostata verlaufen, geschont werden. Das Risiko der postoperativen erektilen Dysfunktion kann damit auf zehn Prozent (bei jungen Patienten), bis 50 % (bei älteren Patienten) gesenkt werden, der Erfolg ist aber signifikant von der Erfahrung des Operateurs abhängig. Zudem birgt die Technik das Risiko einer zu wenig radikalen Ausräumung des Tumors. Es erhöht sich damit das langfristige Risiko eines Lokalrezidives.
Die Art der angewandten Operationsmethode scheint keinen signifikanten Einfluss auf die onkologischen Ergebnisse (Überlebensrate, rezidivfreies Überleben etc.) des Eingriffs zu haben, vielmehr scheint die jeweilige Erfahrung des einzelnen Operateurs ausschlaggebend zu sein.
Strahlentherapie (Radiatio)

Außer beim lokal begrenzten Prostatakrebs (PK) mit niedrigem Risikoprofil kann die Strahlentherapie bei nahezu allen Formen und Stadien des PK angewandt werden. Die Technik, die dabei zum Einsatz kommt, wird meist mit den Kürzeln IMRT + IGRT (Intensitätsmodulierte Radiotherapie + Bildgestützte Bestrahlung – Image Guided Radiotherapy) beschrieben. Mit dieser Technik ist es möglich, von außerhalb des Körpers 3-dimensional gesteuert und kontrolliert die vorgesehene Strahlendosis genau in den Gewebebereich zu platzieren, in dem die Wirkung gewünscht wird. Umliegende Gewebeareale werden dabei weitgehend geschont. Die Strahlentherapie kommt in der Regel zusammen mit anderen Therapieformen zum Einsatz (beispielsweise der Androgendeprivation).[9.10] Eine weitere Form der Strahlentherapie ist die Brachytherapie. Hierbei wird eine Strahlungsquelle mit unterschiedlicher Verweildauer in die Prostata eingebracht. Die abgegebene Strahlung zerstört räumlich begrenzt das umliegende Gewebe. Die Brachytherapie wird in verschiedenen Intensitätsstufen verabreicht, daher die Bezeichnungen LDR-Brachytherapie (LDR für Low Dose Rate) oder HDR-Brachytherapie (HDR für High Dose Rate). Die Brachytherapie wird auch mit der IMRT+IGRT-Technik kombiniert. In diesem Fall wird Strahlung von außen und von innen appliziert.[9.10]
Bei der Strahlentherapie eines PK kann es zu typischen Nebenwirkungen kommen. Insbesondere treten häufig Entzündungen der äußeren Haut (Dermatitis) und der Schleimhaut im Darm (Radioproktitis, Strahlenkolitis) auf. Ferner klagen die Patienten gelegentlich über vorübergehende Übelkeit, Müdigkeit und Abgeschlagenheit. Art und Intensität der Nebenwirkungen hängen in hohem Maße von der Art der Durchführung und Technik der Strahlentherapie ab. Die Behandlung der Nebenwirkungen erfolgt nach allgemeinen pflegerischen Erfahrungen. Eine ausreichende Evidenz für die eine oder andere Behandlungsmethode oder Prophylaxe gibt es nicht.[9.10]
Photodynamische Therapie
In der S3-Leitlinie von 2025 wird die Photodynamische Therapie (vaskulär-gezielte photodynamische Therapie, VDT) als einzige fokale (nur am Tumor wirkende) Therapie bezeichnet, für die Vergleichsstudien mit dem aktiven Beobachten (active Surveillance) vorliegen. In diesen Studien erscheint die VDT dem aktiven Beobachten überlegen zu sein.[9.11] Der für die VDT erforderliche Wirkstoff Padeliporfin ist in Deutschland zugelassen.[41] In der Zulassung wird die Anwendung auf spezielle Krankheitsstadien beschränkt.[42]
Das Wirkprinzip beruht darauf, dass die Substanz Padeliporfin über eine Infusion in den Körper eingebracht wird. Sie führt bei gleichzeitiger Einwirkung von Licht mit einer bestimmten Wellenlänge zum Absterben von Körpergewebe. Nach der Infusion wird der Tumor mit Laserlicht bestrahlt, das Tumorgewebe stirbt ab.[9.12]
Fokale Therapien verfolgen das Ziel der vollständigen Heilung. Ihre Wirkung ist auf einen eng umschriebenen Bereich der Prostata beschränkt, sie gelten daher als minimal-invasive Methode. Sie sind attraktiv, weil sie durch ihre Wirkungsbeschränkung auch wenig unerwünschte Nebenwirkungen verursachen. Verglichen mit den Standardtherapien (perkutane Strahlentherapie, radikale Prostatektomie, LDR-Brachytherapie) sind die Erfahrungen noch relativ gering und die Datenlage eher schlecht.[9.10]
Aktive Überwachung, Strahlentherapie oder Operation: Ergebnisse der britischen ProtecT-Studie
Bis vor Kurzem war nicht eindeutig geklärt, ob Operation oder Strahlentherapie als gleichwertig anzusehen sind; es gab keinen direkten Vergleich beider Therapieverfahren. Ferner war unklar, ob eine Behandlung (egal welche) einen Vorteil gegenüber der aktiven Überwachung erbringt. Die in Deutschland zu dieser Frage durchgeführte PREFERE-Studie wurde im Herbst 2016 geschlossen. Fast zeitgleich wurde aber eine britische Studie veröffentlicht (sog. ProtecT-Studie), in der drei Methoden miteinander verglichen wurden, nämlich aktive Überwachung, Operation und Strahlentherapie (Bestrahlung von außen mit Linearbeschleuniger, kombiniert mit sechsmonatiger antihormoneller Therapie).
Wichtige Ergebnisse der ProtecT-Studie sind:
- Aktive Überwachung ist möglich. Es gibt in den ersten zehn Jahren nach Diagnose keine erhöhte Todesrate.
- Allerdings traten bei Patienten, die zunächst nur überwacht und nicht sofort behandelt wurden, vermehrt Metastasen auf. Da dies längerfristig nachteilig ist, sollte man eine Therapie bei jüngeren Patienten und/oder bei Tumoren mit Risikokonstellation prüfen.
- In der Patientengruppe, die zunächst nur aktiv überwacht wurde, musste man innerhalb von zehn Jahren dann doch die Hälfte der Patienten mit Bestrahlung oder Operation behandeln, weil die Krebserkrankung messbar vorangeschritten war. Bei aktiver Überwachung gilt also bezüglich einer weiteren Behandlung: aufgeschoben, aber nicht endgültig aufgehoben.
- Ein wichtiges Ergebnis betrifft den Vergleich von Operation und Strahlentherapie. Beide Verfahren waren hinsichtlich der Beherrschung der Tumorerkrankung gleich gut (im Trend war die Bestrahlung sogar etwas besser). Beide Therapieverfahren wurden gut vertragen; die Nebenwirkungen waren bei Strahlentherapie aber deutlich geringer als bei Operation, obwohl die Bestrahlung noch nicht mit heute üblichen präziseren Bestrahlungstechniken durchgeführt wurde.
Die beiden Originalpublikationen der Studie,[43] eine Zusammenfassung der österreichischen Cochrane,[44] ein Kommentar aus dem New England Journal of Medicine[45] sowie eine Pressemitteilung der Deutschen Gesellschaft für Radioonkologie[46] sind frei verfügbar. Die Aussagen gelten nur für Patienten mit den entsprechenden Kriterien, insbesondere einem Tumor mit weniger aggressiver Einstufung.
Weitere Ergebnisse zur Frage, welche Behandlungsmethode die besten Erfolgsaussichten bietet, stammen aus der 2012 publizierten sogenannten „Grimm-Studie“. In dieser Metaanalyse wurden anhand der Daten von ca. 52.000 Patienten mit lokalisiertem Prostatakarzinom 11 Methoden (operative Verfahren, Bestrahlungsmethoden, HiFu usw.) untersucht und verglichen. Die besten Ergebnisse bei allen drei Risikogruppen lieferte stets ein Bestrahlungsverfahren. Den ausgeprägtesten Vorteil in Bezug auf die langjährige Tumorkontrolle zeigte die Bestrahlung im Vergleich zur Operation bei Patienten mit Hochrisiko-Prostatakrebs.[34]
Hormontherapie
Die umgangssprachliche Bezeichnung Hormontherapie wird fachlich korrekt als Androgendeprivationstherapie (ADT) bezeichnet. Das Therapieprinzip beruht nämlich nicht auf einer Hormongabe, sondern vielmehr in einer Wirkungsblockade des Sexualhormons Testosteron. Die Wachstumsgeschwindigkeit fast aller Prostatakrebse (PK) hängt vom Testosteronspiegel ab. Mit bestimmten Medikamenten kann man den Testosteronspiegel und damit die Wachstumsgeschwindigkeit des Tumors senken. Der Verlauf lässt sich so über Jahre hinauszögern. Heilen kann man den PK damit nicht.[47] Die ADT kann in verschiedenen Krankheitsstadien eingesetzt werden, meist als Begleitung zur Strahlentherapie oder Chemotherapie. Eine Hormontherapie in Form eines Hormonentzuges kann als (meist reversible) chemische Kastration durch Gabe von GnRH-Agonisten oder -Antagonisten, oder durch operative beidseitige Entfernung der Hoden (bilaterale Orchiektomie) durchgeführt werden.[9.10] Ziel ist es, den Testosteronspiegel auf unter 50 ng/dl abzusenken. Bei allen Verfahren der ADT kommt es meist zu einem deutlichen Rückgang[9.10] bzw. Stillstand der Krankheit, so dass der Patient oft über Jahre keine karzinombedingten Beschwerden hat. Bei der chemischen Kastration mittels GnRH-Agonisten kann ein sogenanntes Flare-up-Phänomen entstehen, ein kurzzeitig stark beschleunigter Krankheitsverlauf, bedingt durch einen kurzzeitigen Anstieg des Testosterons. Dieser kann durch die kurzzeitige Gabe von Antiandrogenen wie Cyproteronacetat unterbunden werden.[47] Aktuelle Studiendaten liefern Hinweise darauf, dass die Therapieoptionen bei Patienten mit kardiovaskulären Erkrankungen sorgfältig abgewogen werden sollten. Darüber hinaus gibt es Studien, die gezeigt haben, dass GnRH-Antagonisten gegenüber den GnRH-Agonisten mit einem deutlich geringeren Risiko für kardiovaskuläre Erkrankungen einhergehen.[48][49]
Als Nebenwirkungen bei allen Kastrationsverfahren kommt es meist zu Testosteronmangelsymptomen. Unter anderem muss mit Hitzewallungen, depressiven Zuständen, Anämie, Muskelabbau, Knochenschmerzen und als Langzeitwirkung Osteoporose gerechnet werden.[47] Bei der Orchiektomie treten sowohl die psychischen Belastungen durch die irreversible chirurgische Kastration als auch die Osteoporose durch das nicht gleichzeitig supprimierte Hormon LH stärker in Erscheinung. Außerdem kommt es zur erektilen Dysfunktion, die meist als nicht allzu schlimm empfunden wird, da auch die Libido nachlässt. Um diese therapiebedingten Nebenwirkungen zu minimieren, kann bei einigen Patienten die intermittierende Hormonblockade (intermittierende Androgendeprivation) zur Anwendung kommen, das heißt, therapiefreie Intervalle werden bewusst eingeplant.[50][51]
Chemotherapie
Die Chemotherapie kommt beim Prostatakrebs (PK) zum Einsatz, wenn sich Metastasen entwickelt haben. In der Regel wird sie zusätzlich zur Hormontherapie angewandt. Sie dient nicht der Heilung, sondern lebensverlängernd. Das Medikament der Wahl ist Docetaxel, in seltenen Fällen wird auch Cabazitaxel verwendet.[9.10][52] Die Chemotherapie hat den Nachteil, dass sie oft mit starken Nebenwirkungen verbunden ist. Beim Präparat Docetaxel sind das: Verminderung der weißen Blutkörperchen (Neutropenie), Verminderung der roten Blutkörperchen (Anämie), Haarausfall (Alopezie), Übelkeit, Erbrechen, Entzündung der Mundschleimhaut (Stomatitis), Durchfall (Diarrhoe), Schwäche (Asthenie) und Veränderungen der Fingernägel (Onychodystrophie).[9.10][52]
Supportive Therapie
Auch wenn eine Heilung nicht möglich ist, kann mit den zur Verfügung stehenden Therapieverfahren meist eine beträchtliche Lebenszeitverlängerung erreicht werden. In dieser Zeit soll die Lebensqualität möglichst wenig eingeschränkt sein. Daher ist es notwendig, die unerwünschten Nebenwirkungen der Behandlung abzumildern.
Allgemeine supportive (unterstützende) Maßnahmen sind regelmäßige körperliche Aktivität und eine gesunde Ernährung mit Schwerpunkt auf pflanzlicher Kost. Es gibt keine Evidenz für den Erfolg der Anwendung von Nahrungsergänzungsmitteln oder von komplementären medizinischen Methoden.[9.13]
Supportive Therapie bei unerwünschten Wirkungen der radikalen Prostatektomie:[9.13]
- postoperative Harninkontinenz: Empfohlen wird eine Physiotherapie mit Kontinenztraining
- erektile Dysfunktion: Bei Bedarf kann eine Therapie mit PDE-5 Inhibitoren durchgeführt werden. Je nach Präferenz können auch Hilfsmittel und Physiotherapie zum Einsatz kommen.
- Anostomosenstriktur: Eine Verengung der Harnröhre an der Nahtstelle nach der radikalen Prostatektomie kann durch wiederholtes vorsichtigen Aufdehnen korrigiert werden. Notfalls wird ein erneuter operativer Eingriff erforderlich.
Supportive Therapie bei unerwünschten Wirkungen der Strahlentherapie:[9.13]
- Die Nebenwirkungen Dermatitis und Proktitis werden nach allgemeinen pflegerischen Grundsätzen behandelt. Die Anwendung von Kortisonpräparaten hat sich in diesem Zusammenhang bewährt. Es liegen jedoch dazu keine wissenschaftlichen Studien vor.[9.13]
Supportive Therapie bei unerwünschten Wirkungen der Hormonentzugstherapie:[9.13]
- Hitzewallungen: Medikamentöse Therapie mit Cyproteronacetat, Antidepressiva, Clonidin
- Gynäkomastie: Der Vergrößerung der Brustdrüsen kann durch Bestrahlung vorgebeugt werden, die operative Entfernung kommt auch in Frage
- Zunahme des Körperfetts, Abnahme der Muskulatur: Hier kann durch körperliche Aktivität und entsprechende Ernährung entgegengewirkt werden
Palliativtherapie
Im fortgeschrittenen Stadium, das keine kurative (heilende) Behandlung mehr erlaubt, können dennoch medizinische Maßnahmen die Beschwerden lindern und die Lebensqualität auf einem passablen Niveau halten. Bisphosphonate wie Zoledronsäure haben sich als wirksam erwiesen, um osteoporotische Veränderungen im Zuge der antiandrogenen Therapie ebenso wie durch Skelettmetastasen hervorgerufene Frakturen zu reduzieren.[53] Zur Linderung der Knochenschmerzen werden Opioide wie Morphin oder Oxycodon eingesetzt. Durch die äußere Bestrahlung von Knochenmetastasen können ebenfalls für einige Zeit die Schmerzen reduziert werden. Die Injektion bestimmter Radioisotope wie Strontium-89, Phosphor-32, Samarium-153 oder Radium-223 (Alpharadin, Xofigo),[54] die sich in stoffwechselaktiven Knochenmetastasen anreichern, hat einen ähnlichen Effekt (siehe Radionuklidtherapie von Knochenmetastasen).
Im Übrigen unterscheidet sich die palliative Therapie beim Prostatakrebs nicht von derjenigen anderer Krebsarten.
Therapieverfahren ohne ausreichende Evidenz
Es gibt mehrere Therapieverfahren, mit denen keine großen Patientenzahlen behandelt worden sind und keine aussagekräftigen Studien durchgeführt wurden (mangelnde Evidenz).
Hochintensiver fokussierter Ultraschall
Ein seit 1996 in Deutschland angewandtes Verfahren ist der hochintensive fokussierte Ultraschall (HIFU). Die Methode beruht darauf, dass die gesamte Prostata vom Enddarm aus mit gerichteten Ultraschallwellen erhitzt und das Karzinom damit zerstört wird. Dazu wird der Schallkopf in das Rektum eingeführt. Die Behandlung erfolgt in einer Sitzung, der Krankenhausaufenthalt beträgt nur drei bis fünf Tage.[55] In der S3-Leitlinie von 2025 wird diese Methode nicht empfohlen.[9.10]
Fokale Kryotherapie
Hierbei wird über eine Hohlnadel Gas in das Prostatagewebe geleitet. Dadurch wird es auf −40 °C abgekühlt. Das Gewebe und mit ihm der Tumor werden so zerstört.[55] In der S3-Leitlinie von 2025 wird diese Methode nicht empfohlen.[9.10]
Irreversible Elektroporation (IRE)
Es werden Elektroden vom Damm aus in die Prostata eingeführt. Eine elektrische Spannung zwischen den Elektroden erzeugt elektromagnetische Felder, welche das Gewebe zerstören. Die Methode ist nicht ausreichend erprobt, es gibt wenig Erfahrungen.[55] In der S3-Leitlinie von 2025 wird diese Methode nicht empfohlen.[9.10]
Immuntherapie
Ein neuer therapeutischer Ansatz ist die „Impfung“ mit antigenpräsentierenden Zellen, die mit einem rekombinanten Fusionsprotein (PA2024) beladen werden und die körpereigene Immunantwort stimulieren. Versuche finden derzeit statt bei Patienten mit androgen-unabhängigem Prostatakarzinom. Diese Patienten konnten bisher nur schwer behandelt werden, da sie auf eine Hormontherapie nicht ansprechen. Diese Behandlung ist in Deutschland nicht zugelassen. In der S3-Leitlinie von 2025 wird diese Methode nicht empfohlen. Es besteht noch weiterer Forschungsbedarf.[9.10]
Weitere Therapien ohne ausreichende Erfahrung zu Wirkung und Nebenwirkung sind: Fokale Laserablation, die fokale Radiofrequenzablation (RFA), die fokale stereotaktische Bestrahlung (SBRT), die fokale Mikrowellentherapie, sowie die fokale transurethrale Ultraschallablation.[9.10]
Phytotherapie
Ein Nutzen sogenannter Phytohormone aus Soja lässt sich nicht belegen, auch isoliert gegebene sekundäre Pflanzenstoffe zeigen keine Wirksamkeit. Fachgesellschaften warnen auch vor Beispielen in der Werbung, deren Wirksamkeit nicht belegt ist (zum Beispiel Lycopin aus Tomaten).[56]
Gegenstand zahlreicher Studien ist Granatapfelsaft, dieser ist der am besten untersuchte Pflanzenstoff bei Prostatakrebs.[57] So sollen die darin enthaltenen phytochemischen Pflanzenstoffe wirksam bei der Senkung des oxidativen Stresses und bei der Modulierung von Entzündungswegen sein.[58] Zudem üben die enthaltenen Substanzen in Zellkultur einen inhibitorischen Effekt auf das Tumorwachstum aus.[59] Im Mittelpunkt steht die Auswertung des PSA-Wertes (prostataspezifisches Antigen), das als zentraler Marker für einen möglichen Therapieerfolg gewertet wird. Die Ergebnisse zahlreicher Studien sind uneinheitlich, es fehlen verlässliche Überlebensdaten.[57] Außerdem ist nicht bekannt, ob sich ein möglicher positiver Einfluss auf den PSA-Wert auf den Tumor auswirkt. Die Datenlage ist zu begrenzt, um Aussagen über eine mögliche Therapieform (als Ergänzung oder als Ersatz für die klassische Therapieform) zu treffen.[56] Ein pauschaler Gebrauch von Granatapfelprodukten bei Patienten mit Prostatakarzinom wird nicht empfohlen. Jedoch ist die Einnahme von Granatapfelsaft nebenwirkungsarm.[59]
Rehabilitation
Nach radikaler Prostatektomie (RPE), Strahlentherapie, Hormontherapie und fokaler Therapie soll den Patienten eine fachspezifische Rehabilitationsbehandlung angeboten werden. Diese soll allgemein der Wiederherstellung der psychischen und physischen Leistungsfähigkeit sowie gegebenenfalls der Wiedereingliederung in das Erwerbsleben dienen.[9.14]
Nach RPE liegt die Zielsetzung auf der Therapie von Harninkontinenz und erektiler Dysfunktion, nach Strahlentherapie eher auf der Behandlung von Funktionsstörungen von Blase und Darm. Patienten nach und während einer Hormontherapie soll Bewegungstraining angeboten werden. Die Zielsetzung besteht hier neben der Steigerung allgemeiner körperlicher Leistungsfähigkeit in der Optimierung des Verhältnisses von Muskel-, Fett-, und Knochenmasse.[9.14]
Nachsorge
Nach den „Patientenleitlinien“ sind Nachuntersuchungen wie folgt vorzunehmen: Im ersten und zweiten Jahr alle drei Monate; im dritten und vierten Jahr alle sechs Monate und ab dem fünften Jahr jährlich. Dies umfasst vor allem regelmäßige Kontrollen des PSA-Wertes. Bildgebende Verfahren werden nur bei entsprechendem klinischen Verdacht auf ein Tumorrezidiv oder eine Krankheitsprogression eingesetzt.
Prognose und Auswirkungen auf die Lebenserwartung
Die Prognose des Prostatakarzinoms ist für eine bösartige Geschwulst beziehungsweise eine Krebserkrankung relativ günstig. Zumindest im lokalisierten Stadium (es wird hier auch illustrierend vom „Haustierkrebs“ gesprochen) ist die Lebenserwartung kaum verkürzt. Man nimmt an, dass letztlich weniger als ein Fünftel der an Prostatakrebs Erkrankten auch an ihm versterben, also die Letalität weniger als 20 % beträgt. Grund hierfür ist die späte Manifestation und die zu diesem Zeitpunkt meist bestehende Komorbidität. In einer Studie konnte gezeigt werden, dass im lokalisierten Stadium die Prognose beim Zuwarten (siehe dazu den Abschnitt „Aktives Beobachten“) nicht schlechter ist als bei sofortiger Therapie.[60] Die hohe Mortalität ist somit vor allem auf die auffallend hohe Prävalenz im höheren Lebensalter zurückzuführen.
Das diagnosespezifische Fünfjahresüberleben nach Diagnosestellung liegt bei Tumoren, die auf die Drüse begrenzt sind, bei 80 bis 99 %.[61] Bei gestreuten Tumoren liegt dieser Wert jedoch mit etwa 30 % deutlich niedriger.[62] Die Aussicht auf Heilung (also darauf, alle Krebszellen zu zerstören) ist nur bei nicht metastasierten Karzinomen gegeben und dort unter aggressiver Therapie recht gut: Auf die Prostata begrenzte Karzinome können zu fast 90 %, die Organkapsel überschreitende zu etwa 50 % definitiv geheilt werden. Bei einem lokal begrenzten Prostatakarzinom liegt die Heilungschance bei etwa 70 %.[63] Zur genaueren Abschätzung der Prognose dienen die so genannten Partin-Tabellen,[64] bei denen eine Kombination aus PSA-Wert, Gleason-Score und T-Stadium zur Prognoseeinschätzung herangezogen wird.
Die hier gemachten Aussagen gelten für das Adenokarzinom der Prostata. Die seltenen neuroendokrinen und kleinzelligen Prostatakarzinome haben eine deutlich schlechtere Prognose mit einer Überlebenszeit von durchschnittlich einem Jahr.
Geschichte
Der älteste bisher nachgewiesene Fall eines metastasierten Prostatakarzinoms wurde anhand von typischen Knochenveränderungen bei einem 2700 Jahre alten Skelett eines Skythen-Fürsten in Sibirien diagnostiziert. Entdecker waren Forscher der Georg-August-Universität Göttingen um Michael Schultz.[65]
Die Vorsteherdrüse wurde zuerst von dem venezianischen Anatom Niccolò Massa im Jahr 1536 beschrieben. Die erste Illustration veröffentlichte Andreas Vesalius zwei Jahre später. Trotzdem war das Prostatakarzinom bis 1853 unbekannt.[66] Aufgrund der schlechten diagnostischen Optionen und der geringeren allgemeinen Lebenserwartung galt es im 19. Jahrhundert als seltene Krankheit. Die ersten Orchiektomien waren schon um 1890 versucht worden, allerdings mit bescheidenem Erfolg. Die ersten operativen Eingriffe an der Drüse selbst zielten auf Verbesserung des Wasserlassens bei Harnröhrenobstruktion. So wurde die erste radikale Prostatektomie 1904 von Hugh Young im Johns Hopkins Hospital durchgeführt.[67] Mitte des 20. Jahrhunderts wurde die palliative transurethrale Resektion (via Harnröhre) zur Behebung der Harnröhrenobstruktion eingeführt. Die radikale retropubische Prostatektomie wurde 1983 von Patrick Craig Walsh entwickelt.
1941 veröffentlichte Charles Brenton Huggins seine Studienergebnisse, in denen er (chemisch gekoppelte) Estrogene einsetzte, um bei Patienten mit inoperablem Karzinom die Testosteron-Produktion zu hemmen.[68] Die Entdeckung dieser „chemischen Kastration“ brachte ihm 1966 den Nobelpreis für Physiologie oder Medizin ein.
Die Strahlentherapie wurde im frühen 20. Jahrhundert entwickelt und bestand zunächst aus der Einpflanzung von Radium-Implantaten. Die perkutane Bestrahlung wurde seit Mitte des Jahrhunderts durchgeführt. Die erste Beschreibung der Brachytherapie stammt aus dem Jahr 1983.
Veterinärmedizin

Bei Haustieren sind Prostatatumoren wesentlich seltener zu finden als beim Menschen. Bei Katzen sind bisher nur fünf Fälle dieser Erkrankung beschrieben worden. Am relativ häufigsten erkranken Hunde. Hier sind etwa 0,2–0,6 % aller Neubildungen Tumoren der Prostata. Unter den Neoplasien der männlichen Harn- und Geschlechtsorgane beim Hund liegt der Anteil bei sechs Prozent. Bevorzugt erkranken Hunde mittelgroßer bis großer Rassen mit einem Altersdurchschnitt von acht bis zehn Jahren. Eine Kastration bewirkt keinen Rückgang der Erkrankungshäufigkeit; es gibt vielmehr Hinweise, dass die Erkrankung bei kastrierten Rüden häufiger auftritt.[69] Die Erkrankung ist differentialdiagnostisch vor allem von der wesentlich häufiger auftretenden gutartigen Prostatavergrößerung des Hundes abzugrenzen. Ein Tumor der Prostata ist beim Hund fast immer eine bösartige Neubildung, in den meisten Fällen handelt es sich wie beim Menschen um Adenokarzinome. Kastrierte Rüden weisen dagegen bei etwa 50 % der Fälle undifferenzierte Karzinome auf. Als weitere bösartige Neoplasien sind Plattenepithelkarzinome, Übergangsepithelkarzinome und Leiomyosarkome sporadisch beschrieben worden. Lediglich Einzelfälle stellen gutartige Fibrome, Adenome oder Leiomyome dar. Entsprechend ihrem aggressiven Charakter liegen zum Zeitpunkt der Diagnosestellung in 70 bis 80 % der Fälle bereits Metastasen vor. Die Verschleppung der Tumorzellen erfolgt über die Lymphbahn und betrifft in 66 % der Fälle die Lunge. Dieser Verlauf scheint bei kastrierten Rüden häufiger zu sein als bei intakten. Außerdem sind von Metastasen die Lymphknoten im Beckenbereich sowie Leber, Milz, Herz, Nieren, entferntere Lymphknoten, Knochen und die Nebennieren betroffen.
Symptome

Das klinische Erscheinungsbild der Erkrankung ist variabel. Kotabsatzstörungen wie Tenesmus oder Obstipation treten wesentlich häufiger als Beschwerden bei der Miktion auf. Die Neubildung kann Schmerzsymptome im Bereich der Hinterhand hervorrufen, die bei Metastasierung in die Wirbelsäule hinein sogar als Lähmungen imponieren können. Auf rektale Palpation treten in einigen Fällen Schmerzhaftigkeiten auf. Eine Vergrößerung des Organs ist jedoch nicht in allen Fällen nachweisbar. Im Urin lassen sich in zwei Dritteln der Fälle Anzeichen für eine Entzündung oder eine Einblutung nachweisen. Tumorzellen selbst werden hier allerdings nur selten gefunden. Eine Verwendung der humanmedizinischen Marker Saure Phosphatase und Prostataspezifisches Antigen ist umstritten, zumal die humanmedizinischen Tests beim Hund nicht angewendet werden können.
Diagnostik
Im Röntgenbild können bei Metastasierung in den betroffenen Organen häufig Veränderungen nachgewiesen werden. Die Prostata selbst ist häufig vergrößert und weist Verkalkungsherde auf. Im Ultraschall ist neben einer Vergrößerung des Organs häufig eine erhöhte Echogenität und in einigen Fällen das Vorhandensein von Zysten nachweisbar. Die definitive Diagnose erfolgt mittels einer transabdominalen oder transrektalen Prostatabiopsie und anschließender pathohistologischer Untersuchung. Eine weitere Möglichkeit besteht in der Durchführung einer Kathetersaugbiopsie, bei welcher mittels eines Harnröhrenkatheters aus dem Bereich der Prostata Zellen angesaugt werden.
Therapie
Da die meisten Hunde mit einem Tumor der Prostata erst beim Vorliegen von Metastasen vorgestellt werden, ist die Prognose in den meisten Fällen von vornherein ungünstig. Früherkennungsmaßnahmen wie zum Beispiel PSA-Tests werden gegenwärtig noch nicht angeboten. Die mittlere Überlebenszeit nach Diagnosestellung liegt bei drei Monaten. Eine chirurgische Entfernung der Prostata ist durch die meist große Ausdehnung des Tumors oft nicht möglich. Bei intakten Rüden wird die Überlebenszeit auch durch eine Kastration oder die Gabe von Antiandrogenen nicht verbessert. Auch verschiedentlich getestete Chemotherapieprotokolle oder Strahlentherapien verbesserten die Prognose nicht nachweislich.
Siehe auch
Literatur
Leitlinien
- Patientenratgeber Prostatakrebs (PDF; 1 MB), Patientenleitlinie Lokal begrenztes Prostatakarzinom (PDF; 1,5 MB), Patientenleitlinie Lokal fortgeschrittenes und metastasiertes Prostatakarzinom (PDF; 1,5 MB) (Deutsche Krebsgesellschaft)
- S3-Leitlinie Prostatakarzinom der Deutschen Gesellschaft für Urologie (DGU). In: AWMF online (Stand 2025)
Fachbücher
- Emil A. Tanagho, Jack W. McAninch: Smith’s General Urology. 17. Auflage. McGraw-Hill Professional, 2008, ISBN 978-0-07-145737-8.
- Oliver W. Hakenberg: Prostatakarzinom. In: Hans-Ulrich Schmelz et al. (Hrsg.): Facharztwissen Urologie: Differenzierte Diagnostik und Therapie. 3. Auflage. Springer, Berlin / Heidelberg 2014, ISBN 978-3-642-44942-0, S. 219–262, doi:10.1007/978-3-642-44942-0_23.
Zeitschriftenbeiträge
- Lothar Weißbach, Jens Altwein: Aktive Überwachung oder aktive Therapie beim lokalen Prostatakarzinom? In: Dtsch. Ärztebl. Int. Nr. 106 (22), 2009, S. 371–376 (Artikel).
- D. G. Bostwick et al.: Human prostate cancer risk factors. In: Cancer, November 2004, Band 101, Nummer 10, Supplement, S. 2371–2490. doi:10.1002/cncr.20408. PMID 15495199. (Review).
Weblinks
- PathoPic – Bilddatenbank der Universität Basel: Adenokarzinom der Prostata (Bild eines Präparates)
- PathoPic – Bilddatenbank der Universität Basel: Tumorinfiltration der Harnblase (Bild eines Präparates)
- Prostatakrebs. In: Zentrum für Krebsregisterdaten. Robert-Koch-Institut, 29. November 2021, abgerufen am 22. Dezember 2021.
- Prostate cancer. National Cancer Institute (englisch).
- Prostatakarzinom. Online-Lehrbuch der Urologie für Ärzte und medizinisches Fachpersonal.
- Prostatakrebs. Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen.
- Patienteninformation Früherkennung von Prostatakrebs. Ärztliches Zentrum für Qualität in der Medizin.
- Präventionsfaltblatt Prostatakrebs erkennen (PDF; 1,3 MB) der Deutschen Krebshilfe.
- Patientenleitlinien Prostatakrebs. Leitlinienprogramm Onkologie, abgerufen am 5. August 2024.
- Arriba PSA Rechner. unter anderem Informationen zur Aussagekraft von positiven und negativen Testergebnissen. Abgerufen am 5. August 2024.