クロロプレン
From Wikipedia, the free encyclopedia
| クロロプレン | |
|---|---|
 |
 |
2-Chlorobuta-1,3-diene | |
別称 Chloroprene, 2-chloro-1,3-butadiene, Chlorobutadiene, β-Chloroprene | |
| 識別情報 | |
| CAS登録番号 | 126-99-8 |
| PubChem | 31369 |
| ChemSpider | 29102 |
| UNII | 42L93DWV3A |
| EC番号 | 204-818-0 |
| 国連/北米番号 | 1991 |
| KEGG | C19208 |
| ChEBI | |
| ChEMBL | CHEMBL555660 |
| RTECS番号 | EL9625000 |
| バイルシュタイン | 741875 |
| Gmelin参照 | 277888 |
| |
| |
| 特性 | |
| 化学式 | C4H5Cl |
| モル質量 | 88.5365 g/mol |
| 外観 | 無色の液体 |
| 匂い | 刺激臭、エーテルのような |
| 密度 | 0.9598 g/cm3 |
| 融点 |
−130 °C |
| 沸点 |
59.4 °C |
| 水への溶解度 | 0.026 g/100 mL |
| 溶解度 | エタノールに溶ける。ジエチルエーテル、アセトン、ベンゼンと混和する。 |
| 蒸気圧 | 188 mmHg (20 °C)[1] |
| 屈折率 (nD) | 1.4583 |
| 危険性 | |
| GHSピクトグラム |    |
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H225, H302, H315, H319, H332, H335, H350, H373 |
| Pフレーズ | P201, P202, P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P271, P280 |
| 主な危険性 | 高い引火性、刺激性、毒性 |
| NFPA 704 | |
| 引火点 | −15.6 °C (3.9 °F; 257.5 K) |
| 爆発限界 | 1.9–11.3%[1] |
| 許容曝露限界 | TWA 25 ppm (90 mg/m3) [皮膚][1] |
| 最低致死濃度 LCLo | 1052 ppm (ウサギ, 8時間) 350 ppm (ネコ, 8時間)[2] |
| 半数致死量 LD50 | 450 mg/kg (ラット, 経口) |
| 半数致死濃度 LC50 | 3207 ppm (ラット, 4時間)[2] |
| 関連する物質 | |
| 関連するジエン | ブタジエン イソプレン |
| 関連物質 | クロロエチレン 2,3-ジクロロブタジエン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
クロロプレン(Chloroprene)は、化学式が CH2=CCl-CH=CH2 のジエンである。IUPAC名は2-クロロ-1,3-ブタジエンである。
無色の液体で、特有の臭気を有する。水に難溶、有機溶媒に易溶。重合して過酸化物を作りやすいため、通常はヒドロキノンやフェノチアジンなどの抑制剤が加えられる。引火性が高く、刺激性も強い。
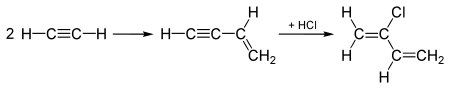
アセチレンの二量化によって得られるビニルアセチレンへの塩化水素の付加,または ブタジエンの塩素化で得られるジクロロブテンの脱塩酸によって合成される。
クロロプレンゴム(ネオプレン)の原料である。