ヒストンH1
From Wikipedia, the free encyclopedia
| linker histone H1 and H5 family | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| 識別子 | |||||||||||
| 略号 | Linker_histone | ||||||||||
| Pfam | PF00538 | ||||||||||
| InterPro | IPR005818 | ||||||||||
| SMART | SM00526 | ||||||||||
| SCOP | 1hst | ||||||||||
| SUPERFAMILY | 1hst | ||||||||||
| |||||||||||
ヒストンH1(英: histone H1)は、真核生物細胞のクロマチンの構成要素となる5つの主要なヒストンタンパク質ファミリーの1つである。ヒストンH1は高度に保存されているものの、生物種間の配列の多様性はヒストンの中では最も高い。
機能
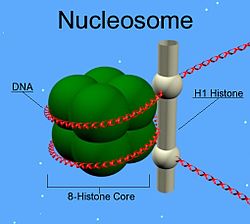
他のヒストンとは異なり、H1はヌクレオソームの「ビーズ」を構成しない。H1はビーズ構造上に位置し、DNAがヌクレオソームの周囲を巻くよう適切な位置に維持している。ヌクレオソームのビーズは4種類のヒストン2分子ずつから構成されるが、H1は1分子である。ヌクレオソームへの結合に加えて、H1タンパク質はヌクレオソーム間の「リンカーDNA」(約20–80ヌクレオチドの長さ)に結合し、ジグザグ型の30 nmクロマチン繊維の安定化を助けている[4]。ヒストンH1に関しては精製されたクロマチン繊維を用いて多くの研究がなされている。天然のクロマチンや再構成されたクロマチンからリンカーヒストンを除去すると、低浸透圧条件下で30 nm繊維からbeads-on-a-string型ヌクレオソームへ高次構造の解消が促進される[5][6][7]。
H1はリンカーDNAの露出部分を短くしてソレノイド状のクロマチン繊維の形成を促進しているのか、それともリンカーの長さには影響を与えることなく単に隣接するヌクレオソームの角度の変化を促進しているだけであるのかは明確ではない[8]。しかしながら、リンカーヒストンは強力な601ヌクレオソームポジショニングエレメントからなる合成DNAを用いてin vitroで再構成されたクロマチン繊維の凝縮を駆動することが示されている[9]。ヌクレアーゼ分解実験やDNAフットプリンティング実験からは、ヒストンH1の球状ドメインはヌクレオソームのダイアド(dyad)部分の近傍に位置していることが示唆されており、ヒストンH1の存在によってさらに約15–30塩基対のDNAが保護される[10][11][12][13]。また、再構成クロマチンを用いた実験では、H1の存在下ではダイアド部分には特徴的なDNAのステムモチーフが生じることが示されている[14]。H1の機能に関しては見解の相違が存在するものの、一般的に受け入れられているモデルは、H1の球状ドメインはヌクレオソームへ入るDNAと出るDNAを架橋して閉じ、テール部分はリンカーDNAに結合してその負電荷を中和する、というものである[8][12]。
H1の機能に関する実験の多くは低塩条件下で精製されプロセシングされたクロマチンを用いて行われているが、in vivoでのH1の役割に関してはさらに不明な点が多い。細胞を用いた研究では、H1の過剰発現は核の形態とクロマチン構造の異常を引き起こすこと、H1は遺伝子によって転写の正の調節因子としても負の調節因子としても作用しうることが示されている[15][16][17]。ツメガエルの卵抽出液では、リンカーヒストンの除去によって分裂期染色体の長さは約2倍となり、過剰発現では染色体は分離不可能な塊へ過剰凝縮される[18][19]。多細胞生物ではH1は複数のアイソフォームがいくつかの遺伝子クラスターとして存在するため、in vivoでのH1の完全なノックアウトは行われていないが、テトラヒメナ、シロイヌナズナ、線虫、ショウジョウバエ、マウスを用いてさまざまなアイソフォームをさまざまな程度で除去する実験が行われており、核の形態やクロマチン構造、DNAメチル化、特定の遺伝子の発現などに生物種特異的なさまざまな欠陥が生じることが示されている[20][21][22]。
ダイナミクス
核内のヒストンH1の大部分はクロマチンに結合している一方で、H1分子はかなり高率でクロマチン間を移行することが知られている[23][24]。
こうした動的なタンパク質がどのようにクロマチンの構造的構成要素となっているのかを理解するのは難しいが、核内での定常状態の平衡はH1とクロマチンの結合がかなり有利であることが示唆されている。このことは、そのダイナミクスにもかかわらず、どの時点においても大多数のH1はクロマチンに結合した状態であることを意味している[25]。H1はDNAに力がかかっている状態やクロマチンの組み立て時において、DNAを圧縮して安定化することが示されており、H1の動的な結合はヌクレオソームを除去する必要がある状況下でDNAを保護していることが示唆される[26]。
クロマチン上でのヒストンH1の動的な交換には細胞質の因子が必要であるようであるが、具体的には未同定である[27]。H1のダイナミクスの一部はO-グリコシル化とリン酸化によって媒介されている可能性がある。H1のO-グリコシル化はクロマチンの凝縮を促進する可能性がある。間期の間のH1のリン酸化はクロマチンに対する親和性を低下させることが示されており、クロマチンの脱凝縮と活発な転写を促進している可能性がある。しかしながら、有糸分裂期のリン酸化はH1の染色体に対する親和性を増大させ、染色体凝縮を促進することが示されている[19]。
アイソフォーム
動物のH1ファミリーには複数のH1のアイソフォームが存在し、それらは生体内で異なる組織と発生段階で発現しているものや、重複した領域で発現しているものもある。こうした複数のアイソフォームが存在する理由は明らかではないが、ウニからヒトまで進化的に保存されていることやアイソフォーム間のアミノ酸配列の大きな差異は、これらが機能的に等価なものではないことを示唆している[3][28][29]。1つのアイソフォームはヒストンH5と呼ばれ、このアイソフォームは鳥類の赤血球にのみ見られる。他のアイソフォームとしては卵母細胞/受精卵型アイソフォームH1M(B4またはH1fooとしても知られる)があり、ウニ、カエル、マウス、そしてヒトにも存在し、胚では体細胞型アイソフォームH1A–Eや、H5に似たH1.0アイソフォームへと置き換えられる[3][30][31][32]。H1Mは体細胞型アイソフォームよりも多くの負電荷を持つにもかかわらず、ツメガエルの卵抽出液中の分裂期染色体に対してより高い親和性で結合する[19]。