クロコン酸
From Wikipedia, the free encyclopedia
| クロコン酸 | |
|---|---|
 | |
 |
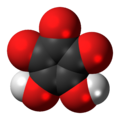 |
別称 4,5-dihydroxycyclopent-4-ene-1,2,3-trione Crocic acid | |
| 識別情報 | |
| CAS登録番号 | 488-86-8 |
| PubChem | 546874 |
| ChemSpider | 476003 |
| |
| |
| 特性 | |
| 化学式 | C5H2O5 |
| モル質量 | 142.07 g mol−1 |
| 融点 |
> 300 °C (dec.) |
| 酸解離定数 pKa | 0.80, 2.24 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
クロコン酸(クロコンさん、croconic acid)は化学式 C5H2O5 または (C=O)3(COH)2 で表される有機酸である。シクロペンテン骨格に2つの水酸基、3つのカルボニル基を持ち、オキソカーボン酸の一種でもある。日光に敏感で[1]、水・エタノールに可溶[2]、黄色結晶性固体で、212 °Cで分解する[3]。
水酸基の水素がプロトンとして脱離することで酸性を示す (pK1 = 0.80 ± 0.08 and pK2 = 2.24 ± 0.01 at 25°C)[4][5]。クロコン酸水素イオン C5HO−
5[1]、クロコン酸イオン C5O2−
5 はどちらも安定である。特にクロコン酸イオンは芳香族性を示し[6]、対称性を持つため、二重結合と負電荷が5つのカルボニル基に非局在化する。リチウム・ナトリウム・カリウム塩は二水和物となるが[7]、橙色のカリウム塩は一水和物の形態もとる[1][4]。アンモニウム・ルビジウム・セシウム塩は無水物となる[7]。バリウム・鉛・銀塩も知られている[1]。
クロコン酸とクロコン酸カリウム二水和物は、1825年にレオポルト・グメリンによって発見された。名はギリシャ語で「サフラン」または「卵黄」を意味するκρόκοςに由来する[7]。クロコン酸アンモニウムの構造は、1964年、Baenzigerらにより決定された。クロコン酸カリウム二水和物の構造は、2001年、J. D. Dunitzにより決定された[8]。
構造
クロコン酸の固体は、4分子のクロコン酸が水素結合でつながることで、特有の蛇腹状構造をとる[7]。これはキュリー温度400 K以上の強誘電体で、有機結晶としては最大の自発分極をもつ (約 20 μC cm−2)。この分極は分子の回転ではなく、プロトンの分子間移動によって起こる[9]。クロコン酸分子の双極子モーメントはかなり大きく、ジオキサン中では9-10 D、分子単体でも7-7.5 Dと推定されている[9]。
アルカリ金属塩においては、クロコン酸イオンと金属イオンは平行に列を形成する[7]。複塩 K3(HC5O5)(C5O5)・2H2Oでは、クロコン酸イオン C5O2−
5 とクロコン酸水素イオン HC5O−
5 の間で水素が共有されていることが示されている[7]。
クロコン酸イオンの非局在化電子は、潜在的にπスタッキングを起こす能力を持つため、超分子化学の観点からも興味が持たれている[10]。
赤外・ラマン分光では、全てのC-C結合長は等しく、その長さは対イオンの半径に影響を受けることが示されている[6]。この結果からは、芳香族性の程度が対イオンの半径の関数となるという解釈が導かれる。同研究において、最適化された構造と振動スペクトルによる量子力学的DFT計算が行われている。この結果、理論的にも、芳香族性が対イオンの半径の増大につれて増加することが示された。
クロコン酸イオンは2価の遷移金属イオンと、一般式M(C5O5)·3H2Oで表される水和錯体を作る。金属イオンによって結晶の色は様々で、銅(褐色)、鉄(暗紫色)、亜鉛(黄)、ニッケル(緑)、マンガン(暗緑色)、コバルト(紫)などである。これらの結晶は全て斜方晶系で、クロコン酸イオンと金属イオンが繰り返した鎖状構造をとる。各クロコン酸は前方の金属イオンに1個、後方の金属イオンに2個の酸素で結合し、もう2個の酸素は結合に関与しない。各金属はこれらの3つのクロコン酸酸素と、1つの水分子に結合する[11]。カルシウムでも同様の組成の固体(黄)が生成するが、結晶構造は異なる[11] 。
3価の遷移金属イオンとは、アルミニウム(黄)、クロム(褐色)、鉄(紫)のような錯体を形成する。これらの結晶も水和水をもつが、その構造は2価の金属イオンよりも複雑である[11]。現在のところ、金属と非局在化した電子が結合するサンドイッチ化合物を形成するという証拠はない[11]。だが、酸素原子が金属と結合するパターンとして、1-5個全ての場合が確認されている[12][13][14]。