メチルリチウム
From Wikipedia, the free encyclopedia
| メチルリチウム | |
|---|---|
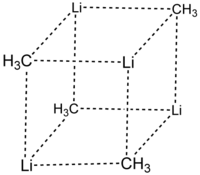 | |
Methyllithium | |
別称 Lithium methanide リチウムメタニド | |
| 識別情報 | |
| CAS登録番号 | 917-54-4 |
| PubChem | 2724049 |
| ChemSpider | 10254338 |
| 日化辞番号 | J1.231I |
| EC番号 | 213-026-4 |
| ChEBI | |
| バイルシュタイン | 3587162 |
| Gmelin参照 | 288 |
| |
| |
| 特性 | |
| 化学式 | CH3Li |
| モル質量 | 21.98 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
メチルリチウム (methyllithium) は化学式 CH3Li で表される有機リチウム化合物である。メチル基を Me と略記し、MeLi とも表記される。溶液中および固体状態では会合体(クラスター)を形成している。反応性が非常に高く、炭化水素溶液やエーテル溶液として有機合成などに用いられる。水や酸素に弱いため、無水・無酸素条件下で取り扱う必要がある。普通は実験室で調製されることはなく、溶液が広く市販されている。
反応
強塩基であると同時に求核性も高い。炭素原子は形式的に負電荷を持ち、求電子剤やプロトン供与剤と反応する。主にメチル化剤、リチオ化剤として使われる。
例えばフェロセンはメチルリチウムで処理するとリチオ化される。有機化学などで溶媒として用いられるテトラヒドロフランとも反応する。水やアルコールとは激しく反応する。メチルリチウムを使った反応は多くの場合大きく発熱的なため、低温で行う必要がある。
メチルリチウムはメチルアニオン等価体として用いられる。ケトンと反応させるとメチル化し、中間体を加水分解すると三級アルコールが得られる。
非金属ハロゲン化物に作用させるとメチル基が導入された生成物を与える。三塩化リンとの反応を例示する。
一般的に上記の目的には、より安全に取り扱うことができ、同等の反応性を有するメチルマグネシウムハライドが用いられる。
メチル基を持つ遷移金属錯体はメチルリチウムを使って合成することができる。








