Ferrate de baryum
From Wikipedia, the free encyclopedia
| Ferrate de baryum | |
  |
|
| Structure du ferrate de baryum | |
| Identification | |
|---|---|
| Nom UICPA | Ferrate(VI) de baryum |
| Synonymes |
Ferrate(2-) de baryum |
| SMILES | |
| InChI | |
| Apparence | Cristaux opaques rouge foncé |
| Propriétés chimiques | |
| Formule | BaFeO4 |
| Masse molaire[1] | 257,17 ± 0,01 g/mol Ba 53,4 %, Fe 21,72 %, O 24,89 %, |
| Propriétés physiques | |
| Solubilité | insoluble |
| Cristallographie | |
| Système cristallin | orthorhombique |
| Classe cristalline ou groupe d’espace | Pnma, No. 62[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le ferrate de baryum est le composé chimique de formule BaFeO4. Il s’agit d’un composé rare contenant du fer à l’état d'oxydation +6[3]. Il est isostructural avec le sulfate de baryum BaSO4 et contient l’anion tétraédrique [FeO4]2−[4].
L’anion ferrate(VI) est paramagnétique en raison de ses deux électrons non appariés et il a une géométrie moléculaire tétraédrique[5].
La diffraction des rayons X a été utilisée pour déterminer les caractéristiques de la maille élémentaire orthorhombique[2] (vecteurs de réseau a ≠ b ≠ c, angles interaxes α = β = γ= 90°)[6] du BaFeO4 nanocristallin. Il cristallise dans le groupe d'espace Pnma (groupe ponctuel : D2h) avec les paramètres de maille a = 0,8880 nm, b = 0,5512 nm et c = 0,7214 nm[2]. La précision des données de diffraction des rayons X a été vérifiée par les intervalles de franges du réseau de la microscopie électronique en transmission à haute résolution (HRTEM) et les paramètres de maille calculés à partir de la diffraction de zone sélectionnée (en) (SAED)[2].
Caractérisation
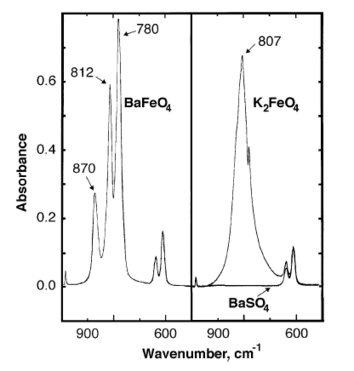
Des pics d'absorption infrarouge du ferrate de baryum sont observés à 870, 812, 780 cm−1[7].
BaFeO4 suit la loi de Curie-Weiss et a un moment magnétique de (2,92 ± 0,03) × 10-23 A m2 (3,45 ± 0,1 BM) avec une constante de Weiss de -89 K[9].
Préparation
Le ferrate de baryum(VI) peut être préparé par des méthodes de synthèse humide ou sèche. La synthèse sèche est généralement réalisée à l’aide d’une technique thermique, par exemple en chauffant de l’hydroxyde de baryum et de l’hydroxyde de fer(II) en présence d’oxygène à environ 800 à 900 °C[10] :
- Ba(OH)2 + Fe(OH)2 + O2 → BaFeO4 + 2 H2O
Les méthodes par voie humide utilisent à la fois des techniques chimiques et électrochimiques. Par exemple, l’anion ferrate se forme lorsqu’un sel de fer approprié est placé dans des conditions alcalines et qu’un agent oxydant puissant, tel que l’hypochlorite de sodium, est ajouté[11] :
- 2 Fe(OH)3 + 3 OCl- + 4 OH- → 2 FeO42- + 5 H2O + 3 Cl-
Le ferrate de baryum est ensuite précipité à partir de la solution par l’ajout d’une solution de sel de baryum[11]. L’ajout d’un sel de baryum soluble à une solution de ferrate de métal alcalin produit un précipité marron de ferrate de baryum, un cristal qui a la même structure que le chromate de baryum et a à peu près la même solubilité[12]. Le ferrate de baryum a également été préparé en ajoutant de l’oxyde de baryum à un mélange d’hypochlorite de sodium et de nitrate ferrique à température ambiante (ou à 0 °C)[13]. La pureté du produit peut être améliorée en effectuant la réaction à basse température en l’absence de dioxyde de carbone et en filtrant et séchant rapidement le précipité, réduisant ainsi la coprécipitation de l’hydroxyde de baryum et du carbonate de baryum en tant qu’impuretés[12].