Oxyde de thallium(III)
From Wikipedia, the free encyclopedia
| Oxyde de thallium(III) | |
| |
| Oxyde de thallium(III) | |
| Identification | |
|---|---|
| Synonymes |
trioxyde de thallium, sesquioxyde de thallium |
| No CAS | |
| No ECHA | 100.013.846 |
| No CE | 215-229-3 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | solide brun foncé |
| Propriétés chimiques | |
| Formule | Tl2O3 |
| Masse molaire[1] | 456,764 8 ± 0,001 3 g/mol O 10,51 %, Tl 89,49 %, |
| Susceptibilité magnétique molaire | +76,0·10−6 cm3/mol |
| Propriétés physiques | |
| T° fusion | 717 °C |
| T° ébullition | 875 °C (se décompose) |
| Solubilité | insoluble |
| Masse volumique | 10,19 g/cm3 |
| Cristallographie | |
| Système cristallin | Cubique |
| Symbole de Pearson | [2] |
| Classe cristalline ou groupe d’espace | Ia3 (No. 206) |
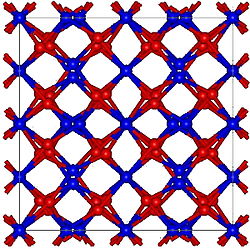
| Structure type | Bixbyite |
| Précautions | |
| SGH[3] | |
| H373, H411, P273, P314, P301+P310+P330 et P304+P340+P310 |
|
| NFPA 704 | |
| Écotoxicologie | |
| DL50 | 44 mg/kg (oral, rat) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'oxyde de thallium(III), appelé également oxyde thallique, est un composé chimique de thallium et d'oxygène. Ils se présente dans la nature sous forme du minéral rare avicennite[4]. Sa structure est apparentée à celle de Mn2O3 qui a une structure de type bixbyite. Tl2O3 est métallique avec une conductivité élevée et est un semi-conducteur dégénéré de type n qui peut avoir une utilisation potentielle dans les cellules solaires[5]. Une méthode de production de Tl2O3 par MOCVD est connue[6]. Toute utilisation pratique de l’oxyde de thallium(III) devra toujours tenir compte de la nature toxique du thallium. Le contact avec l'humidité et les acides peut former des composés toxiques du thallium.




