骨髄像
From Wikipedia, the free encyclopedia


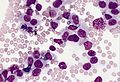
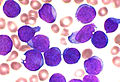
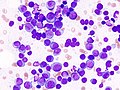
骨髄像(こつずいぞう、英語: Bone marrow smear examination、 myelogram[※ 1])とは、骨髄から得た細胞をスライドガラスに塗抹、染色して顕微鏡で観察する検査である。 末梢血塗抹検査では原則として成熟した血液細胞しか観察できないが、血液細胞は骨髄で産生されて成熟するため、骨髄液塗抹標本では幼若な血液細胞を観察することができる。骨髄像は血液疾患の診断、病期判定、治療効果判定などに不可欠な場合が多い。 また、血液疾患以外でも、悪性腫瘍の転移、感染症、先天性代謝異常などに関する重要な情報を得られる場合がある。
通常、骨髄穿刺を行い、0.2から0.3 mL[※ 2]の骨髄液を吸引してスライドガラスに塗抹し染色した標本を顕微鏡で観察する。 同時に、液中の有核細胞数や巨核球数を計測し、骨髄像検査の一環として併せて報告する(有核細胞数の項参照)[※ 3]。
穿刺液が十分に得られない場合(ドライタップと呼ばれる)、穿刺針や骨髄生検標本などをスライドガラスに捺印して染色する場合もある[1]。
染色は、通常、形態観察用にメイ・グリュンワルド・ギムザ染色などのロマノフスキー染色が行われるが、必要に応じ、鉄染色など、後述の特殊染色が追加される。
標本の観察にあたっては、異常細胞の検出、造血能の評価、末梢血塗抹標本との対比、等を念頭において観察するとともに、 通常は、有核細胞[※ 4]の分画を算定する[※ 5]。
検査の適応
骨髄穿刺は患者への負担が大きいので、 診療の必要上、病歴・身体診察・末梢血等の一般的な検査では不十分な場合にのみ実施される[※ 6]。 以下、骨髄穿刺の適応となる病態の例をあげる[2]:253-268。
血液疾患の診断
白血球分画で分画の異常や異常細胞の出現、末梢血塗抹検査での血球形態異常などから血液疾患が疑われた場合、 確定診断目的で骨髄像検査が行われることが多い。
- 血液系の腫瘍性疾患の診断
急性白血病、各種の骨髄増殖性腫瘍(慢性骨髄性白血病、真性多血症、等)などについては、 通常、全血球計算や末梢血塗抹検査での異常から血液疾患を疑い、骨髄像検査が実施される。
多発性骨髄腫、原発性マクログロブリン血症などの免疫グロブリン系疾患については、アルブミン/グロブリン比(A/G比)や血清蛋白分画などから疑われて、血清・尿のM蛋白 (単クローン性蛋白)の検索とともに骨髄検査を施行することが多い。
悪性腫瘍の広範な骨髄転移(骨髄癌腫症[※ 7])は末梢血での赤芽球や幼若白血球の出現(白赤芽球症)がきっかけになって骨髄穿刺にいたり診断がつく場合が多い[3]。
- 各種の血球減少症・増多症の診断
全血球計算で原因不明の血球数の異常(貧血/多血症、白血球増多/減少、血小板増多/減少)、特に、複数の系統の血球数の異常が見られた場合に、診断確定のため骨髄像検査が実施される。 例としては、再生不良性貧血、骨髄異形成症候群などがあげられる。
悪性腫瘍の病期診断
悪性リンパ腫やホジキン病では骨髄浸潤の頻度が高い[※ 8]。骨髄に腫瘍細胞が認められたら進行期(Ⅳ期)と判断される。
血液疾患の治療効果の監視
化学療法後の残存病変の検索や、造血幹細胞移植後の生着の確認に使用される[2]:253-268。
その他の全身性疾患の検索
骨髄病変を伴う全身性疾患の診断に骨髄像が有用な場合がある[2]:253-268。
- 不明熱
- 不明熱(原因不明の持続性の発熱)の原因検索には骨髄像が重要である。
骨髄像で深在性真菌症、結核、リーシュマニアなどの感染症が診断されることがある(特にHIV感染患者)。また、悪性リンパ腫等、悪性腫瘍の浸潤が発見される場合がある[4]。
有核細胞の分類
骨髄塗抹標本では、通常、500個の有核細胞を目視で同定して分類する[7]。 この分類を指して骨髄像という場合もある。
骨髄像の基準値
骨髄像の基準値は文献や施設により異なるが、一例を示す。
| 骨髄像 | 範囲 (%) | 基準範囲 (%) | メジアン (%) | 平均 (%) | ||
|---|---|---|---|---|---|---|
| 赤芽球系 (E) | 赤芽球 (小計) | 8.5–56.5 | 15.8–46.2 | 32.0 | 31.7 | |
| 前赤芽球 | 0–5.0 | 0–3.0 | 0.5 | 0.6 | ||
| 好塩基性赤芽球 | 0–21.0 | 0.5–13.5 | 3.5 | 4.5 | ||
| 多染性赤芽球 | 3.0–47.0 | 7.8–34.5 | 20.0 | 20.2 | ||
| 正染性赤芽球 | 0–21.0 | 0.5–16.5 | 5.5 | 6.3 | ||
| 骨髄系 (M) | 顆粒球系 (G) | 顆粒球 (小計) | 24.5–72.5 | 34.8–66.3 | 49.5 | 49.9 |
| 好中球 | ||||||
| 骨髄芽球 | 0–8.5 | 0–5.0 | 1.5 | 1.6 | ||
| 前骨髄球 | 0–8.5 | 0–5.5 | 1.0 | 1.3 | ||
| 骨髄球 | 1.0–31.7 | 5.8–24.0 | 13.5 | 13.7 | ||
| 後骨髄球 | 0.5–18.0 | 1.0–12.0 | 4.5 | 5.0 | ||
| 桿状核球 | 2.0–34.0 | 6.5–26.2 | 14.5 | 15.2 | ||
| 分葉核球 | 1.0–27.5 | 2.5–19.7 | 9.5 | 9.8 | ||
| 好酸球 | 0–18.0 | 0.5–7.0 | 2.5 | 3.0 | ||
| 好塩基球 (および マスト細胞)[※ 10] | 0–3.0 | 0–1.5 | 0 | 0.3 | ||
| G/E比(顆粒球系/赤芽球系比) | 0.5–5.9 | 0.8–4.1 | 1.6 | 1.7 | ||
| 単球系 | 単球 | 0–8.5 | 0–6.0 | 2.0 | 2.2 | |
| M/E比(骨髄系/赤芽球系比) | 0.6–6.2 | 0.8–4.1 | 1.6 | 1.8 | ||
| リンパ系 | リンパ球 | 1.0–38.5 | 5.5–23.2 | 13.2 | 13.6 | |
| 形質細胞 | 0–17.5 | 0–7.0 | 2.3 | 2.6 | ||
- この表では、M/E比は「単球系を含めた骨髄系(顆粒球系+単球系)と赤芽球系の比」、G/E比は「顆粒球系と赤芽球系の比」という意味で使用しているので留意されたい。
顆粒球系幼若細胞
白血球系の幼若細胞の大半を占める顆粒球(主に好中球、他に少数の好酸球・好塩基球)の形態の概要を示す[10]。
なお、血液細胞は、一般に、幼若なものほど、細胞が大きく、核は類円形に近く、核クロマチンが繊細で、細胞質の好塩基性(青色調)が強い。 成熟に従い、核は固有の形をとり、クロマチンは粗になり核小体も消失、細胞質も固有の色調を呈し、顆粒球系では特異的な顆粒が出現してくる[11]。
| 顆粒球系 | シェーマ・画像 | 直径 | 核 | 細胞質 | |
|---|---|---|---|---|---|
| 骨髄芽球 (myeloblast) |
 |
10~15μm | 円形、クロマチンは網状繊細、核小体がある。 | 青色、顆粒は認めない。 | |
| 前骨髄球 (promyelocyte) |
 |
15~20μm | 偏在、円形、クロマチンは繊細、核小体を認めることが多い。 | 青色、アズール顆粒(一次顆粒)、核周明庭(ゴルジ野)[※ 11]がみられる。 | |
| 骨髄球 (myelocyte) |
 |
12~20μm | 類円形、クロマチンは粗。核小体は認めない。 | 特異顆粒(二次顆粒)を認める、青色が薄れる。アズール顆粒は残存していることがある。 | |
| 後骨髄球 (metamyelocyte) |
 |
12~18μm | 陥凹(腎ないしそら豆型)、クロマチンは粗で一部塊状。 | ほとんどが特異顆粒で占められる | |
赤芽球系幼若細胞
| 赤芽球系 | シェーマ・画像 | 直径 | 核 | 細胞質 | |
|---|---|---|---|---|---|
| 前赤芽球 (proerythroblast) |
①核小体 ②核周明庭 (ゴルジ野) |
20~25μm | 核クロマチンは顆粒状繊細で核小体がある。 | 濃青色、狭く明瞭な核周明庭[※ 11]を認める。 | |
| 好塩基性赤芽球 (basophilic erythroblast) |
16~20μm | 核クロマチンは顆粒状、核小体はない。 | 濃青色、前赤芽球に比べて濃い。核周明庭も認める。 | ||
| 多染性赤芽球 (polychromatic erythroblast) |
 |
 |
12~18μm | 核クロマチンは粗大、一部塊状。核小体はない。 | 淡青色にヘモグロビン色調(橙紅色)が加わる。 |
| 正染性赤芽球 (orthochromic erythroblast) |
8~10 μm | 核クロマチンは濃縮。 | 正常赤血球とほぼ同じ色。 | ||
その他の細胞




- マスト細胞(組織肥満細胞)
- マスト細胞は、骨髄の造血幹細胞・骨髄系前駆細胞に由来するが、骨髄ではなく末梢組織で成熟し、アレルギー反応や自然免疫などに関与する。健常人では血中には出現しない。マスト細胞の核は円形で、好塩基球に似て多数の好塩基性顆粒をもつ[2]:159。
- マクロファージ
- マクロファージ(大食細胞、組織球)は、胎生期に卵黄嚢で発生し各組織に定着した前駆細胞に由来する他、骨髄で成熟した単球も末梢血から組織に移行してマクロファージに分化する。マクロファージは、老化・死滅した細胞などを貪食する他、自然免疫や抗原提示に関与する。マクロファージは大きな細胞で径は15〜80 μmに達し、卵円形の核をもち、細胞質の色は淡く、しばしば貪食した残渣を含む [2]:159-161[14][15]:253。
M/E比
有核細胞分画を算定する場合はM/E比(英語: Myeloid-to-erythroid ratio)も算出される。これは、骨髄の有核細胞のうち、赤芽球系と顆粒球(好中球・好酸球・好塩基球)系の細胞数比率を意味するのが通常である(リンパ球、形質細胞などは除く。なお、単球を含める場合をM/E比、含めない場合をG/E比としている文献もあるので注意を要する[9])。 基準値は「骨髄像の基準値」の項に記載したように0.8〜4.1であるが、文献により、2〜3[16]、1.5〜3.3[17]、2〜4[13]、等、差がある。
- M/E比が上昇する病態
- 赤芽球系造血が低下する病態(赤芽球癆など)、および、顆粒球系が増加する病態(炎症、急性骨髄性白血病、顆粒球コロニー刺激因子(G-CSF)投与など)があげられる。
有核細胞数・巨核球数
骨髄穿刺吸引液中の有核細胞数[※ 4]や巨核球数は骨髄での造血状況を反映し、骨髄像検査の際に併せて算定されるのが通常である。 有核細胞数が低下していると低形成(造血能の低下)、上昇していると過形成(造血能の亢進または異常細胞の増加)と判定する[13][17]。 ただし、骨髄穿刺吸引液には末梢血が混入することが避けられないため、基準値は、おおよその目安程度の位置づけとなる[8]。
| 有核細胞数の基準値[16][8][17][13] | 低値をしめす病態の例 | 高値をしめす病態の例 |
|---|---|---|
| 10万 〜 25万 /μL |
|
骨髄穿刺吸引液中の巨核球数は血小板造血能を反映するが、有核細胞数と同様、末梢血混入の影響が大きい。
| 巨核球数の基準値[16][8][17][13] | 低値をしめす病態の例 | 高値をしめす病態の例 |
|---|---|---|
| 50 〜 150 /μL |
|
特殊染色(血液細胞化学染色)


骨髄細胞の特殊染色としては、血液細胞化学染色(細胞の形態を保ったままで化学反応を行い反応産物を呈色させる検査)がおこなわれる。 主な目的は、鉄などの細胞内物質の検出、および、細胞系統の同定(骨髄系かリンパ系か等)や細胞の分化度の判定、である[※ 13][8][17]。
- 鉄染色
- 鉄染色は、赤芽球やマクロファージの細胞内の非ヘモグロビン鉄[※ 14]をフェロシアンイオンと結合させることにより不溶性の色素ベルリン青(プルシアンブルー)を生成させ、濃青色の鉄顆粒を染め出すものである[※ 15]。赤芽球のおよそ30%は鉄染色で鉄顆粒を認め、鉄芽球と呼ばれる。鉄芽球数は貯蔵鉄量に比例し、鉄欠乏状態では減少するため、貯蔵鉄の評価(鉄欠乏・鉄過剰)に有用である。また、病的状態では、核を囲むミトコンドリア内に病的な鉄顆粒が出現し、これを環状鉄芽球とよぶ。環状鉄芽球の検出は鉄芽球性貧血や骨髄異形成症候群の診断に有用である[17]。
- ペルオキシダーゼ染色(ミエロペルオキシダーゼ染色)
- 好中球や単球に存在するミエロペルオキシダーゼ[※ 16]を検出する染色である。リンパ系細胞にはミエロペルオキシダーゼが含まれないため、古くから急性白血病の芽球がリンパ系か骨髄系かの鑑別に用いられてきており、芽球の3 %以上がミエロペルオキシダーゼ陽性であれば骨髄系と判定する[※ 17][17]。
- エステラーゼ染色
- エステラーゼ反応は単球系細胞と好中球系細胞の鑑別に有用である。単球では非特異的エステラーゼ反応は強陽性であり、好中球では陰性である。なお、T細胞系でも非特異的エステラーゼ反応が弱いながら陽性になるが、単球系ではフッ化ナトリウムによる阻害試験で陰性化する一方、T細胞系では陰性化されないので鑑別可能である[17][13]。
- PAS(パス)染色
- PAS染色は過ヨウ素酸シッフ反応でグリコゲンを染色するもので、正常赤芽球は陰性が通常であるが、急性赤白血病(AML-M6)や骨髄異形成症候群の赤芽球では陽性になることがある。また、骨髄に転移した腺癌細胞では強陽性を示す。ただし、本法は多くの細胞系統で陽性となり特異性が低いため、近年はあまり行われない[17][16]。
骨髄像の異常と病態


- 有核細胞数の増加・減少
- 著減している場合(骨髄低形成)は再生不良性貧血、化学療法後、低形成性白血病[※ 12]などが考えられる。逆に、著増している場合(骨髄過形成)は、急性白血病(低形成の場合もある)、骨髄増殖性腫瘍/疾患、骨髄異形成症候群、溶血性貧血などが考えられる。
- 血球形態異常
- 巨赤芽球性貧血では、巨赤芽球(大型で核が未熟な赤芽球)がみられる。
- 骨髄異形成症候群では、下記のような各系統の細胞形態の異常が見られる[18]。
- 赤芽球系:巨赤芽球、多核赤芽球など。また、鉄染色で環状鉄芽球、PAS染色でPAS染色陽性赤芽球がみられることがある[18]。
- 顆粒球系:アウエル小体、過分葉・ペルゲル・フェット核異常などの核の分葉異常、細胞質顆粒の減少など、さまざまな異形成の所見が見られる。
- 巨核球系:微小巨核球、単核巨核球、分離多核巨核球などの巨核球の形態異常がみられることがある
- 異常細胞や微生物の存在
- 悪性腫瘍の骨髄浸潤、血球貪食症候群の血球貪食像、ゴーシェ病・ニーマンピック病などの先天代謝異常で異常な代謝産物の蓄積した細胞(ゴーシェ細胞、ニーマンピック細胞、泡沫細胞など)がみられることがある[※ 9]。また、感染症の所見や原因微生物がみられることがある。その他の全身性疾患の検索の項を参照されたい。
血液疾患と骨髄像
主要な血液疾患でみられる骨髄像の所見を下の表に示す。
| 急性白血病 | 芽球(白血病細胞)が増加(WHO分類では20 %以上[※ 19]、FAB分類では30 %以上)。 |
| 骨髄異形成症候群 | 通常は正形成から過形成、三系統の細胞(赤芽球系、顆粒球系、巨核球)の形態異常。 |
| 慢性骨髄性白血病 | 顆粒球系を中心に過形成が著明。M/E比上昇。 |
| 真性多血症 | 過形成(赤芽球、顆粒球、巨核球の増加)。 |
| 悪性リンパ腫 | 腫瘍細胞の浸潤がみられることがある(進行期であることを意味する。) |
| 多発性骨髄腫 | 形質細胞の増加がみられる。 |
| 再生不良性貧血 | 有核細胞数が減少。相対的にリンパ球、形質細胞、マクロファージが増加。 |
| 鉄欠乏性貧血 | 赤芽球過形成がみられることが多い。鉄染色では赤芽球などの鉄顆粒が減少している。(本疾患診断のために骨髄検査を行うことは、通常はない。) |
| 悪性貧血 | 巨赤芽球性変化と過形成がみられる。好中球の過分葉がみられる。(骨髄検査は診断のためには必須ではない。) |
| 溶血性貧血 | 赤芽球過形成がみられる。(通常は骨髄検査は必要ない。) |
| 骨髄線維症 | 骨髄液を採取できないことが多い(ドライタップ)。骨髄生検標本で判定する。 |
| 特発性血小板減少性紫斑病 | 巨核球数は正常か増加。(通常は骨髄検査は必要ない。) |
| 本態性血小板血症 | 巨核球数増加(形態異常もみられることがある)。 |
|
|
|
関連する骨髄検査
骨髄生検
細胞の形態学的観察には塗抹標本による骨髄像が優れているが、 骨髄の細胞密度や細胞分布の評価、線維化の評価、悪性腫瘍の転移の組織診断、 などの目的には骨髄生検が優れている。患者の負担は骨髄穿刺よりはやや大きい。 造血能の評価や悪性腫瘍の検索など、病態によっては、骨髄穿刺吸引と骨髄生検が併用されることがある。
骨髄液の遺伝子・染色体検査
白血病などの造血器腫瘍においては、 骨髄像での形態学的観察が診断の基本であることには変わりないが、 近年は病型診断・予後予測・治療方針の決定(治療薬の選択)に遺伝子・染色体検査が不可欠なものとなっている。 1976年に発表された白血病のFAB分類は骨髄像の形態学的観察に基づくものであり、 今日でも形態学的診断の基盤であるが、 分子遺伝学の進歩により、各腫瘍の生物学的性質を把握することが可能となり、 形態学と遺伝学を統合した2001年のWHO分類提案に至った(2025年の時点では、WHO分類の最新版は2024年8月刊行の第5版である)[19][20][7][21][22]。
- G分染法
- G分染法はギムザ染色で染色体の欠失や転座などを調べる方法である。染色体全体の異常を網羅的に可視化でき、複雑な染色体異常も検出できるが、検査には生きた細胞を培養する必要があり、一般に、結果が出るまでに時間を要する。また、検出感度は低く、微量の腫瘍細胞の検出には不向きである[23][17]。
- FISH法
- FISH法は蛍光色素で標識したDNAプローブ(標的遺伝子と相補的な塩基配列をもつDNA断片)をハイブリダイゼーションして観察する方法である。固定後の細胞でも実施可能であり、G分染法に比べ結果が出るのが早いが、プローブを用意する必要があるため、特定の異常の可能性を予想した場合にしか使用できない。
- FISH法の応用例としては、慢性骨髄性白血病の90から95 %にみられる、フィラデルフィア染色体と呼ばれる22番染色体 (ヒト)と9番染色体の間での相互転座の検出があげられる(これにより病因となるBCR-ABL1融合遺伝子が構成されている)[17]。
- PCR法
- PCR法は、各疾患に特徴的な遺伝子変異や融合遺伝子をPCR反応を用いて検出する方法であり、病型診断と治療方針の決定に不可欠になってきている[※ 20]。
- また、10-5から10-6レベルのごく微量の腫瘍細胞を検出可能であり、治療後に光学顕微鏡レベルで寛解と判断された後も残存している腫瘍細胞(微小残存病変)の検出に重要な役割を果たす[16][8]。
- サザンブロット法
- サザンブロット法は、リンパ系の腫瘍を疑う例で、免疫グロブリン(IgH)遺伝子やT細胞レセプター(TCR)遺伝子の再構成のクローナリティ(細胞集団がいくつのクローンに由来するか)の検出に用いられる。腫瘍性疾患ではモノクローナルな増殖が認められる[16]。
骨髄液の細胞表面マーカー検査
細胞表面マーカー検査(フローサイトメトリー)は、 細胞表面の特定の抗原を識別することにより、腫瘍細胞の免疫表現型を知る検査である。 形態学的観察では困難な細胞系統の同定や病型診断、少数の異常細胞の検出、微小残存病変の評価などに有用である。 また、一般に、遺伝子・染色体検査よりも早く結果が出ることが多い。 例をあげれば、急性白血病が骨髄性かリンパ性かの区別はペルオキシダーゼ染色がもちいられるが、 一部のペルオキシダーゼ陰性の急性骨髄性白血病例には骨髄系の細胞表面マーカーであるCD13、CD33の検索が有用である[24]。