ナプロキセンを始めとして、NSAIDs の中には、プロピオン酸系と呼ばれる一連の化合物群がある。それらはいずれもプロピオン酸の 2位が芳香環で置換された構造を持つ光学活性化合物で、S体に望ましい生理活性があることが知られている。そのため、S体の 2-置換プロピオン酸を立体選択的に得るべく、多くの研究が成されてきた。以下、ナプロキセンのラセミ体の光学分割法、および S体の立体選択的合成法について、一例ずつ紹介する。
工業的に用いられた大量合成法を下の図に示す[1]。2-ナフトールから出発して
- Br2による二臭素化
- 亜硫酸水素ナトリウムによる部分還元
- ウィリアムソン合成によるメチル化
- グリニャール試薬に変換後、2-ブロモプロピオナートとのカップリング
以上の段階を経て、ナプロキセンのラセミ体が得られる。これに、N-アルキルグルカミン(グルコースと N-アルキルアミンとの還元的アミノ化により合成)ともう一種類のアミンを 0.5 当量ずつ作用させると、ほぼ (S)-ナプロキセンと N-アルキルグルカミンとの塩のみが不溶物として沈殿する。これを濾過で取り、中和すると (S)-ナプロキセンが得られる(光学純度 >95%)。ろ液では、アミンの作用により (R)-ナプロキセンをラセミ化させることができるため、ここから同様にして再び (S)-ナプロキセンの塩を取り出すことができる。なお、このような光学活性カルボン酸の光学分割の手法は、Pope-Peachey法[2]と呼ばれる。

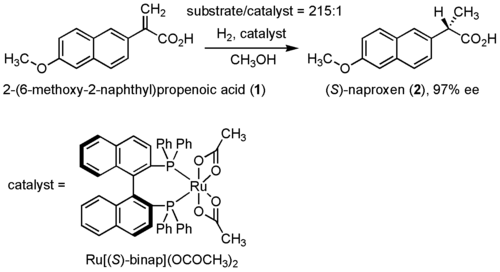
S体の 2-アリール置換プロピオン酸はまた、不斉合成の標的化合物ともされた。ナプロキセンを合成する場合は下図のように、2-(6-メトキシ-2-ナフチル)プロペン酸 (1) のプロキラルなアルケン部位に対し、図の手前側から水素を付加できれば (S)-ナプロキセン (2) が得られる。
野依らは 1987年に、彼らが開発した配位子、BINAP を持つルテニウム錯体 Ru((S)-binap)(OCOCH3)2 を不斉触媒とし、これと水素ガスを用いた不斉水素化により、(S)-ナプロキセン (2) を定量的に、かつ鏡像体過剰率 97%ee と高選択的に得ることに成功した[3]。
その後、K. T. ワン、M. E. デービスにより、水溶性を付与した Ru-BINAP 系触媒をエチレングリコール溶液として担持した親水性の多孔質を用いて、シクロヘキサン/クロロホルム溶媒との二相系による同様の不斉水素化が開発され、その中でも (S)-ナプロキセンの選択的合成が達成された (96%ee)[4]。


