ペンタセン
From Wikipedia, the free encyclopedia
 | |
 | |
| 物質名 | |
|---|---|
Pentacene | |
別名 2,3:6,7-Dibenzanthracene | |
| 識別情報 | |
3D model (JSmol) |
|
| バイルシュタイン | 1912418 |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.004.722 |
| EC番号 |
|
| Gmelin参照 | 733903 |
PubChem CID |
|
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| 性質 | |
| C22H14 | |
| モル質量 | 278.354 g·mol−1 |
| 外観 | 暗青色の固体 |
| 密度 | 1.3 g cm−3 |
| 融点 | 271 °C |
| 沸点 | 350 °C(分解)[1] |
| 磁化率 | -205.4 × 10−6 cm3 mol−1 |
| 構造 | |
| 三斜晶系 | |
| P-1 | |
ペンタセン (pentacene) は5つのベンゼン環が直線状に縮合した多環芳香族炭化水素である。光や酸素に敏感である。ペンタセンは暗青色の粉末だが、酸化すると緑色を帯びるようになる。普通、市販されているものは、外側の層が酸化されているため緑がかっている。ペンタセンの精製には、真空昇華あるいは吸着クロマトグラフィーが利用される。
合成法
初めて実用的な合成法が開発されたのは1961年のことで、ブルックナーとトマスによるものである。フタルアルデヒドをシクロヘキサン-1,4-ジオンを脱水縮合させてペンタセンキノンとし、これをアルミニウムアマルガムで還元することにより、ペンタセンを得る[4]。

その後、ペンタセンの薄層を調製する必要が生じると、前駆体から小分子を脱離させる手法を用いて合成されるようになった。高温でエチレン、テトラハロゲノベンゼン[5]または水[6]を、あるいは光照射により一酸化炭素を脱離させる方法[7]が報告されている。下に150°Cに加熱して一酸化炭素を脱離させ、ペンタセンを得る反応を示す[1]。この方法では、前駆体がクロロホルムなどに溶けやすいためスピンコーティング法と相性がよい。ペンタセンは一般的な有機溶媒には溶けにくいが、1,2,4-トリクロロベンゼンのようなハロゲン化芳香族炭化水素系溶媒中に高温では溶けることが知られている。そこから小さな平板を形成させるために結晶化することができる。

誘導体
ペンタセンは一見アントラセンのような芳香族化合物と類似するように見えるが、その芳香族性に関しては完全には明らかになっておらず、母体ペンタセンとその誘導体は研究対象になっている。
6-メチルペンタセンには互変異性体である6-メチレン-6,13-ジヒドロペンタセンとの間の平衡が存在する。

この平衡は完全にメチレン化合物側に偏っている。この化合物の溶液を200°Cに加熱すると、赤紫色に着色することから、少量のペンタセンが生じていることがわかる。ある研究によれば、この平衡に関わる反応機構は分子内の1,5-ヒドリド転位ではなく、フリーラジカルを含む2分子間の水素移動であるとされている[8]。一方、6-メチルペンタセンの中央部分を取り出した形を持つイソトルエンの場合では、芳香族であるトルエンのほうが安定である。
ペンタセンは1,2,4-トリクロロベンゼン溶媒中で単体硫黄と反応し、ヘキサチアペンタセンを与える[9]。X線結晶構造解析によるとすべての炭素−硫黄間の結合距離がほぼ等しいことから (170pm)、共鳴限界式 A よりも、完全に電荷が分極した B と C の寄与のほうが大きいとされている。

結晶中においては芳香環どうしのπ-π相互作用によってスタッキングしている。隣接する分子上の硫黄原子間の距離は337pmであり、ファンデルワールス半径 (180pm) の和よりも小さい。
類似する化合物であるテトラチアフルバレンと同様、この化合物は有機半導体の分野で研究されている。
アセンは剛直な平面状の分子のように見えるかもしれないが、下に示すようにかさ高い置換基が導入されたものは曲がった構造を持つ[10]。
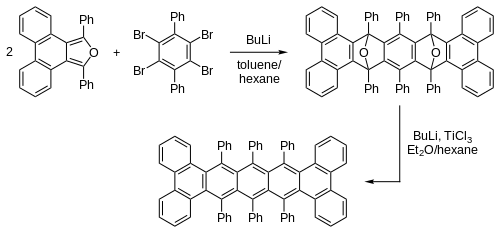
6つのフェニル基により、この化合物の両端はねじれており、二面角は144°である。2つの光学異性体(エナンチオマー)を分離することもでき、それぞれ7400°の旋光度を持つ。エナンチオマーは半減期9時間でラセミ化する。

