酸化エルビウム(III)
From Wikipedia, the free encyclopedia
 | |
 | |
| 物質名 | |
|---|---|
別名 Erbium oxide, erbia | |
| 識別情報 | |
3D model (JSmol) |
|
| ChemSpider | |
| ECHA InfoCard | 100.031.847 |
| EC番号 |
|
PubChem CID |
|
CompTox Dashboard (EPA) |
|
| |
| |
| 性質 | |
| Er2O3 | |
| モル質量 | 382.56 g/mol |
| 外観 | ピンク色の結晶 |
| 密度 | 8.64 g/cm3 |
| 融点 | 2,344 °C (4,251 °F; 2,617 K) |
| 沸点 | 3,290 °C (5,950 °F; 3,560 K) |
| 不溶 | |
| 磁化率 | +73,920·10−6 cm3/mol |
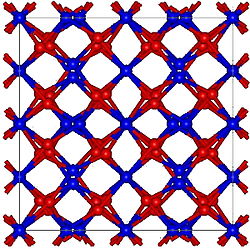
| 構造 | |
| 立方、cI80 | |
| Ia-3, No. 206 | |
| 熱化学 | |
| 標準定圧モル比熱, Cp⦵ | 108.5 J·mol−1·K−1 |
| 標準モルエントロピー S⦵ | 155.6 J·mol−1·K−1 |
標準生成熱 (ΔfH⦵298) |
−1897.9 kJ·mol−1 |
| 関連する物質 | |
| その他の 陰イオン |
塩化エルビウム(III) |
| その他の 陽イオン |
酸化ホルミウム(III)、酸化ツリウム(III) |
酸化エルビウム(III)(さんかエルビウム)は、ランタノイド金属であるエルビウムから合成される。1843年にカール・グスタフ・モサンデルにより部分的に分離され、1905年にジョルジュ・ユルバンとチャールズ・ジェームスにより初めて純粋な形で得られた[2]。ピンク色で立方晶構造をとる。特定の条件下では、酸化エルビウムは六角形の構造をとることもある[3]。